题目内容
6.利用实验器材(规格和数量不限),能完成相应实验的一项是( )| 实验器材(省略夹持装置) | 相应实验 | |
| A | 烧杯、玻璃棒、蒸发皿 | 硫酸铜溶液的浓缩结晶 |
| B | 烧杯、玻璃棒、胶头滴管、滤纸 | 用盐酸除去硫酸钡中的少量碳酸钡 |
| C | 烧杯、玻璃棒、胶头滴管、试剂瓶 | 用固体氯化钠配制一定溶质质量分数的溶液 |
| D | 锥形瓶、水槽、集气瓶、导管、分液漏斗 | 用双氧水和二氧化锰制取并收集氧气 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据硫酸铜溶液的浓缩结晶需要酒精灯进行分析;
B、根据用盐酸除去硫酸钡中的少量碳酸钡,需要过滤操作,要用到漏斗进行分析;
C、根据称量氯化钠的质量需要天平进行分析;
D、根据过氧化氢溶液制取氧气的装置进行分析.
解答 解:A、硫酸铜溶液的浓缩结晶,应加热蒸发水分,所需实验器材有酒精灯、蒸发皿、玻璃棒、铁架台、坩埚钳等;题目提供的实验器材无法完成该实验,故A错误;
B、硫酸钡难溶于水,盐酸会将碳酸钡溶解,可采取加盐酸、过滤、洗涤、干燥的方法进行分离除杂,所需实验器材有烧杯、玻璃棒、漏斗、滤纸、铁架台等;题目提供的实验器材无法完成该实验,故B错误;
C、用氯化钠配制5%的溶液,首先计算配制溶液所需要氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解;在这些操作中需要的实验器材:托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒;题目提供的实验器材无法完成该实验,故C错误;
D、过氧化氢溶液制取的反应物是固体和液体,反应条件是常温,所以题中所给的仪器可以完成,故D正确.
故选:D.
点评 本题难度不大,熟练掌握常见化学实验基本操作的原理、所需仪器等是正确解答本题的关键.

练习册系列答案
相关题目
3.如图所示,烧杯中盛有80℃的热水,杯底放有一小粒白磷,当将一支大试管迅速插入水中并罩住白磷时,白磷立即燃烧起来.该实验说明燃烧需要( ) 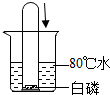

| A. | 水 | B. | 氧气 | C. | 可燃物 | D. | 温度达到着火点 |
1.下列实验操作中,正确的是( )
| A. |  收集CO2 | B. |  量取5 mL水 | ||
| C. |  稀释浓硫酸 | D. |  烧杯中的液体加热 |
16.实验室的药品是按物质分类的方式存放,四个药品柜,已存放了下列药品,现学校实验室新购进一瓶硝酸,正确存放它的药品柜是( )
| 药品柜 | 甲柜 | 乙柜 | 丙柜 | 丁柜 |
| 药品 | 铜、锌 | 红磷、硫 | 氢氧化钠、氢氧化钙 | 盐酸、硫酸 |
| A. | 甲柜 | B. | 乙柜 | C. | 丙柜 | D. | 丁柜 |

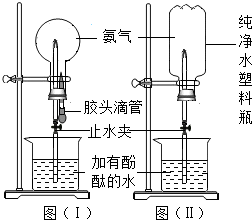
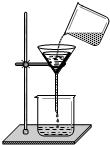 某化学研究性学习小组,为除去粗盐中的Ca2+、Mg2+、Fe3+、$SO_4^{2-}$以及泥沙等杂质,设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
某化学研究性学习小组,为除去粗盐中的Ca2+、Mg2+、Fe3+、$SO_4^{2-}$以及泥沙等杂质,设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量): 现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如下关系:
现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如下关系: 实验室制取氧气的装置如图所示.
实验室制取氧气的装置如图所示.