题目内容
17.硅酸钠(Na2SiO3)是我国优先发展的精细化工产品,其工业制备的反应为:2NaOH+SiO2═Na2SiO3+H2O.现以100t石英砂(SiO2的质量分数为90%)为原料,与足量的NaOH溶液反应来制备Na2SiO3.试计算:
(1)100t石英砂中SiO2的质量为90t.
(2)Na2SiO3中钠、氧元素的质量比为23:24.
(3)理论上可得到硅酸钠的质量(写出计算过程及结果).
分析 根据提供的数据和反应的化学方程式可以进行相关方面的计算.
解答 解:(1)100t石英砂中SiO2的质量为:100t×90%=90t,
故填:90.
(2)Na2SiO3中钠、氧元素的质量比为:(23×2):(16×3)=23:24,
故填:23:24.
(3)设生成硅酸钠的质量为x,
2NaOH+SiO2═Na2SiO3+H2O,
60 122
90t x
$\frac{60}{90t}$=$\frac{122}{x}$,
x=183t,
答:理论上可得到硅酸钠的质量是183t.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目
5.加热胆矾固体的实验过程中,操作正确的是( )
| A. |  取样 | B. |  加药 加药 | C. |  加热 | D. |  熄灭 |
1.为了除去物质中的杂质(括号内物质为杂质),不能达到除杂目的是( )
| 物质 | 选用试剂 | 操作方法 | |
| A | 氧化钙(碳酸钙) | 高温加热 | |
| B | 氮气(氧气) | 灼热的铜网 | 气体通过 |
| C | 硫酸铜溶液(硫酸) | 过量的氧化铜 | 加入氧化铜充分反应后过滤 |
| D | 氯化钠溶液(碳酸钠) | 过量氯化钙溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
2.元素周期表中,氟元素的信息如图所示.下列解释不正确的是( )
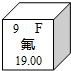

| A. | 原子序数是9 | B. | 氟是非金属元素 | ||
| C. | 质子数是19 | D. | 相对原子质量是19.00 |
 在如图的装置中,当两种物质发生反应后,天平不在保持平衡,指针向右偏转,则该反应遵守质量守恒定律(填“遵守”或“不遵守”).
在如图的装置中,当两种物质发生反应后,天平不在保持平衡,指针向右偏转,则该反应遵守质量守恒定律(填“遵守”或“不遵守”).
