题目内容
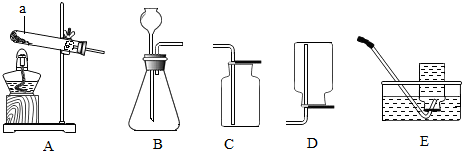
8.甲同学设计了如下实验装置验证一氧化碳的部分性质并验证产物.实验时,在点燃B处酒精灯之前先通入一氧化碳排出装置中的空气,然后继续实验.
①CO气体在使用或点燃前要进行检验气体的纯度;C中反应的化学方程式是CO2+Ca(OH)2→CaCO3↓+H2O;
②实验过程中,B中的现象是黑色固体变成红色,该反应的化学方程式是CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;D处点燃的目的是燃尽CO,防止污染空气;
③对该实验的分析正确的是Ⅰ、Ⅳ(选填编号)
Ⅰ.实验结束时应先熄灭B处酒精灯
Ⅱ.C中增加的质量与B中固体减少的质量相等
Ⅲ.反应开始后通入0.1mol一氧化碳可生成0.1mol铜
Ⅳ.反应结束后继续通入一氧化碳的目的是防止铜被氧化
④甲同学认为A为C的对照实验,通过A、C现象的不同证明B装置中有CO2生成,
乙同学认为省略A可达到同样的目的,理由是点燃酒精灯前,已经先通一段时间CO,可知CO通过澄清石灰水没有明显现象.
⑤通过上述实验可以知道一氧化碳的化学性质是还原性、可燃性.
分析 根据已有的一氧化碳还原氧化铜的知识进行分析解答,一氧化碳能与氧化铜反应生成铜和二氧化碳,其中一氧化碳具有还原性;一氧化碳是有毒的气体,需要进行尾气处理,根据一氧化碳和氧化铜反应的注意事项以及物质的量的关系进行解答即可.
解答 解:①CO气体在使用或点燃前要进行验纯,以防爆炸;
②一氧化碳能与氧化铜反应生成铜和二氧化碳,生成的二氧化碳气体与C中的澄清石灰水发生反应生成白色沉淀碳酸钙和水,其反应方程式为:CO2+Ca(OH)2→CaCO3↓+H2O;
③A中的液体是排除二氧化碳气体;CO通入灼热的氧化铜,将其黑色氧化铜还原为红色的铜单质,并有二氧化碳气体生成,其反应方程式为:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;因为CO具有毒性,所以在D处将多余的CO点燃,防止污染空气;
Ⅰ.实验结束时应先熄灭B处酒精灯,正确;
Ⅱ.C中增加的质量是二氧化碳的质量,B中固体减小的质量是氧元素的质量,故质量不相等,错误;
Ⅲ.该反应前后都要通入一氧化碳,故反应开始后通入0.1mol一氧化碳不可生成0.1mol铜,错误;
Ⅳ.反应结束后继续通入一氧化碳的目的是防止铜被氧化,正确;
④省略A可达到同样的目的,因为为了排尽装置内的空气,反应前已经通入一段时间的CO,故填:为了排尽装置内的空气,反应前已经通入一段时间的CO;
⑤在B处,一氧化碳能还原氧化铜,说明了说明CO有还原性,CuO有氧化性;D处一氧化碳能燃烧,说明了一氧化碳具有可燃性.
故答案是:①检验气体的纯度;CO2+Ca(OH)2→CaCO3↓+H2O;
②黑色固体变成红色;CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;燃尽CO,防止污染空气;
③Ⅰ、Ⅳ;
④点燃酒精灯前,已经先通一段时间CO,可知CO通过澄清石灰水没有明显现象;
⑤还原性、可燃性.
点评 本题考查的是一氧化碳还原氧化铜的知识,完成此题,可以依据已有的知识结合物质的性质进行.

 阅读快车系列答案
阅读快车系列答案| A. | 氧气:氧化性 | B. | 氯化钠:可溶性 | C. | 稀有气体:稳定性 | D. | 碳酸:酸性 |
| A. | H2O+CO2→H2CO3 | B. | 2NaOH+CuSO4→Cu(OH)2↓+Na2SO4 | ||
| C. | 2H2O2$\stackrel{MnO_2}{→}$2H2↑+O2↑ | D. | C+H2O$\stackrel{高温}{→}$H2+CO |
| A. | 该气体的组成可能有2种情况 | B. | 该气体可能是CO和H2 | ||
| C. | 该气体不可能是纯净物 | D. | 该气体一定含有CH4 |
| A. | 降低温度能使任何不饱和溶液转化为饱和溶液 | |
| B. | 升高温度或增大压强均可以增大气体在水中的溶解度 | |
| C. | 将200g质量分数为10%的氯化钠溶液稀释到5%,需要加水200g | |
| D. | 在溶液中加入KNO3晶体和蒸发溶液中的水分这两种方法,都能把8%的KNO3溶液变浓 |