题目内容
8.根据如图所示实验分析得出的结论中,不正确的是( )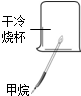 | 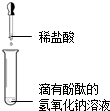 | 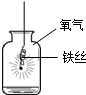 | 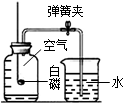 |
| A.甲烷燃烧生成二氧化碳和水 | B.盐酸与氢氧化钠 反应 | C.铁能在氧气中 燃烧 | D.空气中氧气约占 体积的$\frac{1}{5}$ |
| A. | 甲烷燃烧生成二氧化碳和水 | B. | 盐酸与氢氧化钠反应 | ||
| C. | 铁能在氧气中燃烧 | D. | 空气中氧气约占体积的$\frac{1}{5}$ |
分析 A、根据甲烷燃烧能生成二氧化碳和水结合实验现象分析;
B、根据稀盐酸和氢氧化钠反应,使碱性消失分析;
C、根据铁丝能与氧气反应生成四氧化三铁分析;
D、根据测定氧气的原理分析.
解答 解:A、使用干冷的烧杯只能证明甲烷燃烧生成水,不能证明生成二氧化碳,故结论错误;
B、氢氧化钠使酚酞试液变成红色,滴加稀盐酸,红色会褪去,说明碱性消失,证明二者发生了反应,故结论正确;
C、铁丝在氧气中剧烈燃烧,火光四射,有力地证明了铁能在氧气中燃烧,故结论正确;
D、白磷燃烧消耗氧气,该实验现象是进入集气瓶中的水约占瓶体积的$\frac{1}{5}$,说明氧气在空气中氧气的体积分数约为$\frac{1}{5}$,故结论正确;
故选项为;A.
点评 本题考查了学生通过实验现象分析的能力,通过解答本题告诉学生不但要会做实验,更要学会观察,分析现象,得出正确的结论.

练习册系列答案
相关题目
18.将一定量的苯(C6H6)和氧气置于一个完全密闭的容器中引燃,反应后生成二氧化碳、水和一种未知物X.测得反应前后各物质的质量如下表:
下列判断错误的是( )
| 物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 6.6 | 2.7 | m |
| A. | 物质X由碳、氢元素组成 | |
| B. | 物质X为氧化物 | |
| C. | 表中m的值为4.2 | |
| D. | 生成二氧化碳和水的分子个数比为1:1 |
19.生活中有太多的物质变化.下列“变化”中和其他三个不相同的是( )
| A. | 树根变根雕 | B. | 葡萄变美酒 | C. | 玉石变印章 | D. | 玩具机器人变形 |
3.某同学在探究X、Al、Cu三种金属的活动性顺序,分别取溶质质量分数相同的稀盐酸,大小、性状都相同的某金属X、Al、Cu进行实验,实验现象如下:
回答下列问题:
(1)实验开始时,铝表面几乎无气泡产生的原因是,请分析产生这种现象的原因.
(2)由实验现象分析,三种金属的活动性由弱到强的顺序是Cu<X<Al.
(3)若金属X的活动性比铁弱,且金属X与稀盐酸反应后生成易溶于水的XCl2.向只含有XCl2、CuCl2两种溶质的溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中加入稀盐酸,没有气泡产生.则滤液中一定含有的金属阳离子是什么?(用离子符号表示).
| Al | X | Cu | ||
| 现象 | 开始时 | 几乎无气泡产生 | 产生气泡速度较慢 | 无气泡产生 |
| 一段时间后 | 产生气泡速度较快 | 产生气泡速度较慢 | 无气泡产生 |
(1)实验开始时,铝表面几乎无气泡产生的原因是,请分析产生这种现象的原因.
(2)由实验现象分析,三种金属的活动性由弱到强的顺序是Cu<X<Al.
(3)若金属X的活动性比铁弱,且金属X与稀盐酸反应后生成易溶于水的XCl2.向只含有XCl2、CuCl2两种溶质的溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中加入稀盐酸,没有气泡产生.则滤液中一定含有的金属阳离子是什么?(用离子符号表示).
13.工业上用甲、乙制备化学肥料丙,同时生成丁.根据下图得出的结论中,不正确的是( )
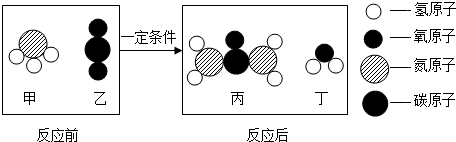

| A. | 甲的化学式为NH3 | B. | 乙和丁属于氧化物 | ||
| C. | 丙中氮元素质量分数约为23.3% | D. | 反应中的甲和乙分子个数比为2:1 |
17.下列物质中,属于纯净物的是( )
| A. |  蒸馏水 | B. |  白酒 | C. |  加碘盐 | D. |  食用醋 |
18.某学习小组测定实验室里一瓶NaOH溶液是否变质,以及变质程度,进行了下列实验,实验方案正确的是( )
| A. | 取少量样品,加入几滴酚酞溶液,溶液由无色变红色,证明氢氧化钠溶液没有变质 | |
| B. | 取少量样品,加入少量稀盐酸,没有气泡产生,证明氢氧化钠溶液没有变质 | |
| C. | 取少量样品,加入过量的氯化钡溶液,有白色沉淀生成,过滤,向滤液中加入几滴酚酞溶液,溶液不变色,证明氢氧化钠溶液完全变质 | |
| D. | 取少量样品,加入过量的氢氧化钡溶液,有白色沉淀生成,过滤,向滤液中加入几滴酚酞溶液,溶液由无色变红色,证明氢氧化钠溶液部分变质 |