题目内容
3.某同学在探究X、Al、Cu三种金属的活动性顺序,分别取溶质质量分数相同的稀盐酸,大小、性状都相同的某金属X、Al、Cu进行实验,实验现象如下:| Al | X | Cu | ||
| 现象 | 开始时 | 几乎无气泡产生 | 产生气泡速度较慢 | 无气泡产生 |
| 一段时间后 | 产生气泡速度较快 | 产生气泡速度较慢 | 无气泡产生 |
(1)实验开始时,铝表面几乎无气泡产生的原因是,请分析产生这种现象的原因.
(2)由实验现象分析,三种金属的活动性由弱到强的顺序是Cu<X<Al.
(3)若金属X的活动性比铁弱,且金属X与稀盐酸反应后生成易溶于水的XCl2.向只含有XCl2、CuCl2两种溶质的溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中加入稀盐酸,没有气泡产生.则滤液中一定含有的金属阳离子是什么?(用离子符号表示).
分析 我们在判断金属活动性的强弱的时候,所进行的操作通常有两种方法:一是让金属与酸反应,然后根据反应的速率即产生气泡的快慢来进行判断,反应越剧烈活泼性越强,二是把一种金属放入另一种金属的盐的溶液中,看是否能够置换出溶液中的金属,来判断它们的活动性,本题可以根据这两个要素来答题.
解答 解:(1)铝是比较活泼的金属,在常温下就能够和氧气反应在表面形成致密的氧化铝薄膜,对铝起到了保护作用.
故答案为:铝表面有一层氧化铝薄膜.
(2)根据与盐酸反应产生气泡的速度可以判断出这三种金属的活动性,产生气泡快的活动性强.
故答案为:Cu<X<Al.
(3)金属X的活动性比铁弱,铜的活动性也比铁弱,所以把铁加入XCl2、CuCl2两种溶质的溶液中时,铁能够把这两种物质都置换出来,注意在反应时总是把最不活泼的全部置换出来之后才能置换较活泼的金属,这是解本题的关键.本题中向滤出的固体中加入盐酸没有气泡产生,说明X没有被置换出来,铁由于发生了置换反应而生成了亚铁离子.
故答案为:Fe2+、X2+
点评 本题考查学生对于金属活动性顺序的探究,我们可以把这类题目归结为“明知故问”型的题目,我们在解答该类题目时就是根据已经掌握的金属活动性顺序,然后选择合适的酸或者是盐的溶液来进行解答

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
13.氨气在化学工业中用途广泛.一定条件下,合成氨反应的微观过程如图所示.下列说法正确的是( )
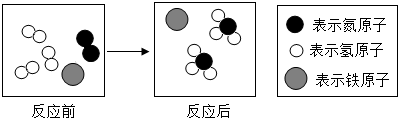

| A. | 该反应属于置换反应 | |
| B. | 参加反应的反应物的微粒数之比为3:1:1 | |
| C. | 该反应中分子总数减少,因此物质的总质量也减少 | |
| D. | 该反应中氢元素化合价升高了,氮元素化合价降低了 |
11.将下列少量物质分别放入水中,充分搅拌,可以得到无色溶液的是( )
| A. | 高锰酸钾 | B. | 面粉 | C. | 汽油 | D. | 氯化钠 |
18.下列验证试验不能成功的是( )
| A. | 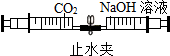 CO2能与烧碱溶液反应 | B. | 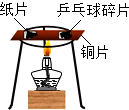 不同物质的着火点不同 | ||
| C. | 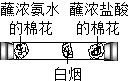 分子在不断运动 | D. | 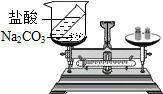 质量守恒定律 |
8.根据如图所示实验分析得出的结论中,不正确的是( )
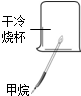 | 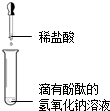 | 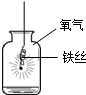 | 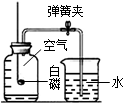 |
| A.甲烷燃烧生成二氧化碳和水 | B.盐酸与氢氧化钠 反应 | C.铁能在氧气中 燃烧 | D.空气中氧气约占 体积的$\frac{1}{5}$ |
| A. | 甲烷燃烧生成二氧化碳和水 | B. | 盐酸与氢氧化钠反应 | ||
| C. | 铁能在氧气中燃烧 | D. | 空气中氧气约占体积的$\frac{1}{5}$ |
12.“单中心铁”可作甲烷高效转化的催化剂,该转化的微观示意图如图,有关转化的说法不正确的是( )
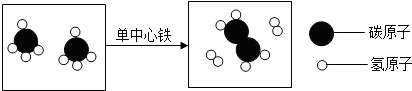

| A. | 反应物和生成物均属于有机物 | |
| B. | “单中心铁”在反应前后质量不变 | |
| C. | “单中心铁”加快了上述反应的速率 | |
| D. | 反应前后原子总数一定没有发生变化 |
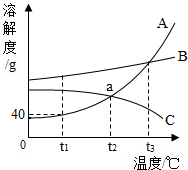 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答: