题目内容
18.将一定量的苯(C6H6)和氧气置于一个完全密闭的容器中引燃,反应后生成二氧化碳、水和一种未知物X.测得反应前后各物质的质量如下表:| 物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 6.6 | 2.7 | m |
| A. | 物质X由碳、氢元素组成 | |
| B. | 物质X为氧化物 | |
| C. | 表中m的值为4.2 | |
| D. | 生成二氧化碳和水的分子个数比为1:1 |
分析 根据质量守恒定律可知:反应后质量减少的物质是反应物,质量增加的物质是生成物;根据质量守恒定律可以确定X的质量;通过计算苯、氧气、二氧化碳、水中各元素的质量,推算出X中所含元素的种类.
解答 解:由表格信息可知反应后CO2质量增加了6.6g,是生成物;H2O质量增加了2.7g,是生成物;O2质量减少了9.6g,是反应物;苯的质量减少了3.9g,是反应物;生成物还少4.2g,所以X是生成物.
B、反应物是苯和O2,生成物是CO2、H2O和X,不是分解反应,故选项错误.
A、根据反应前后元素质量相等,苯中含碳元素的质量为3.9g×$\frac{72}{78}$=3.6g,二氧化碳中含有碳元素的质量为6.6g×$\frac{12}{44}$=1.8g,物质X含有碳元素的质量为3.6g-1.8g=1.8g.苯中含氢元素的质量为3.9g×$\frac{6}{78}$=0.3g,2.7g水中含氢元素的质量为2.7g×$\frac{2}{18}$=0.3g,反应前后氢元素的质量相等,故物质X不含有氢元素.则X中含氧元素的质量为:4.2g-1.8g=2.4g;X中含有C、O两种元素;故错误.
B、由A分析可以看出X是由两种元素组成,其中一种是氧元素,所以属于氧化物;故正确;
C、由上面的分析可以看出:反应后生成的物质x的质量4.2g,故m的值为4.2g,故正确.
D、由上在的分析可求出生成二氧化碳和水的分子个数比为:$\frac{6.6g}{44}:\frac{2.7g}{18}$=1:1;故正确;
由于题目要求选出错误的,故答案为:A.
点评 本题难度不是很大,解答本题要认真分析各物质的质量变化情况,仔细推敲,即可求解.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案
相关题目
8.今年3.15期间,媒体报道了市面上一些不法厂商使用的调和汽油中含甲缩醛,会污染环境.甲缩醛化学式为CH2 (OCH3)2,有关甲缩醛的说法正确的是( )
| A. | 属于氧化物 | |
| B. | 所含碳元素的质量分数为6.2% | |
| C. | 由三个非金属构成 | |
| D. | 1个分子由3个碳原子、8个氢原子和2个氧原子构成 |
9.河南名吃“第一楼小笼包子”以选料讲究,制作精细被誉为“中州膳食一绝”.下列用到的食材中富含糖类的是( )
| A. | 瘦肉 | B. | 小麦粉 | C. | 小磨香油 | D. | 食盐 |
13.氨气在化学工业中用途广泛.一定条件下,合成氨反应的微观过程如图所示.下列说法正确的是( )
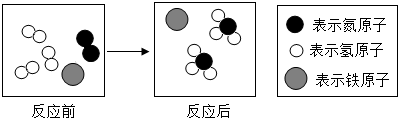

| A. | 该反应属于置换反应 | |
| B. | 参加反应的反应物的微粒数之比为3:1:1 | |
| C. | 该反应中分子总数减少,因此物质的总质量也减少 | |
| D. | 该反应中氢元素化合价升高了,氮元素化合价降低了 |
3.下列各组物质按单质、氧化物、混合物顺序排列( )
| A. | 氮气、氯酸钾、钢 | B. | 氧气、水、澄清石灰水 | ||
| C. | 可燃冰、干冰、冰水混合物 | D. | 石墨、熟石灰、石油 |
10.硫酸亚铁铵晶体俗称摩尔盐,化学式为FeSO4•(NH4)2SO4•6H2O,在制药、电镀方面有广泛的应用.某化学兴趣小组的学生用含有少量铜的废铁屑制备硫酸亚铁铵晶体,流程如图:
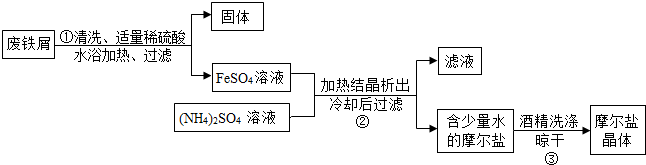
资料:①硫酸亚铁铵晶体易溶于水,不溶于酒精;硫酸亚铁铵晶体在100℃~110℃时分解.
②相关物质的溶解度(单位:g)如下表:
请回答下列问题:
(1)实验前,先用碳酸钠溶液浸泡废铁屑表面油渍.碳酸钠溶液可除去油渍是因为碳酸钠溶液的pH>7(选填“>”、“<”或“=”).
(2)①中发生反应的化学方程式为Fe+H2SO4=FeSO4+H2↑.
(3)操作①中过滤时,要趁热进行的原因是防止过滤时溶液温度降低硫酸亚铁结晶析出,过滤后得到的固体中一定含有的物质是铜(或Cu).
(4)操作③中使用无水酒精洗涤,可快速晾干.这样做的优点是AB(填字母).
A.避免用水洗涤所造成的晶体损耗 B.酒精易挥发,可低温晾干晶体.

资料:①硫酸亚铁铵晶体易溶于水,不溶于酒精;硫酸亚铁铵晶体在100℃~110℃时分解.
②相关物质的溶解度(单位:g)如下表:
| 温度/℃ | FeSO4 | (NH4)2SO4 | FeSO4•(NH4)2SO4•6H2O |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78 | 28.1 |
(1)实验前,先用碳酸钠溶液浸泡废铁屑表面油渍.碳酸钠溶液可除去油渍是因为碳酸钠溶液的pH>7(选填“>”、“<”或“=”).
(2)①中发生反应的化学方程式为Fe+H2SO4=FeSO4+H2↑.
(3)操作①中过滤时,要趁热进行的原因是防止过滤时溶液温度降低硫酸亚铁结晶析出,过滤后得到的固体中一定含有的物质是铜(或Cu).
(4)操作③中使用无水酒精洗涤,可快速晾干.这样做的优点是AB(填字母).
A.避免用水洗涤所造成的晶体损耗 B.酒精易挥发,可低温晾干晶体.
7.推理是一种重要的化学思维方法,以下推理合理的是( )
| A. | 水和双氧水的组成元素相同,所以它们的化学性质相同 | |
| B. | 离子是带电的原子或原子团,所以带电的粒子一定是离子 | |
| C. | 碱溶液呈碱性,所以呈碱性的溶液都是碱溶液 | |
| D. | 化合物是由不同种元素组成的,所以只含一种元素的物质一定不是化合物 |
8.根据如图所示实验分析得出的结论中,不正确的是( )
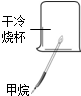 | 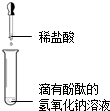 | 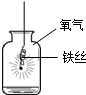 | 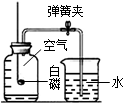 |
| A.甲烷燃烧生成二氧化碳和水 | B.盐酸与氢氧化钠 反应 | C.铁能在氧气中 燃烧 | D.空气中氧气约占 体积的$\frac{1}{5}$ |
| A. | 甲烷燃烧生成二氧化碳和水 | B. | 盐酸与氢氧化钠反应 | ||
| C. | 铁能在氧气中燃烧 | D. | 空气中氧气约占体积的$\frac{1}{5}$ |