题目内容
9.某混合气体可能含有一氧化碳、氢气及少量的二氧化碳和水蒸气和甲烷,某兴趣小组为验证混合的成分,设计了如图所示的装置,进行有关的实验探究【提示:假定每步均完全反应或吸收】.请回答有关问题: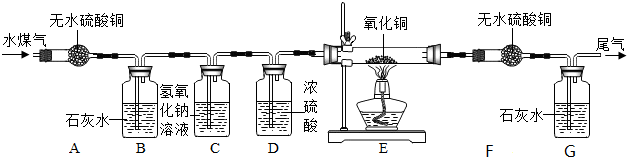
(1)A装置的目的是检验是否含有水.
(2)B中的澄清石灰水变浑浊说明混合气体中含有二氧化碳.
(3)C装置的作用是除去原来的二氧化碳气体.
(4)D装置的作用是除去水蒸气.
(5)同学们对通过D后的可燃气体继续进行探究.若F中无水硫酸铜白色粉末不变蓝,G中的澄清石灰水变浑浊,则可燃气体中一定含有一氧化碳.若F中无水硫酸铜白色粉末变蓝,G中的澄清石灰水不变浑浊,则可燃气体中一定含有甲烷.若F中无水硫酸铜白色粉末变蓝,G中的澄清石灰水变浑浊,请用表中实验数据进行分析,可燃气体的组成有2种.
| 称量项目 | 反应前 | 反应后 |
| F玻璃管及所盛固体的质量 | 86.3g | 89.9g |
| G洗气瓶和所盛石灰水的质量 | 284.2g | 293.0g |
分析 (1)根据水能使白色硫酸铜变蓝分析,
(2)根据二氧化碳能使澄清石灰水变浑浊分析;
(3)根据用氢氧化钠溶液吸收二氧化碳分析;
(4)根据浓硫酸具有吸水性解答;
(5)根据水能使白色硫酸铜变蓝,二氧化碳能使澄清石灰水变浑浊分析.
解答 解:(1)水能使白色硫酸铜变蓝,先通过无水硫酸铜是检验是否含有水;故填:检验是否含有水;
(2)二氧化碳能使澄清石灰水变浑浊,再通过石灰水是检验是否含有二氧化碳的,B中的澄清石灰水变浑浊说明混合气体中含有二氧化碳,故填:二氧化碳;
(3)通过氢氧化钠是除去原来的二氧化碳气体,故填:除去原来的二氧化碳气体;
(4)前面的装置A是为了检验是否有水生成,后面的装置A是为了检验是否有水生成,从而确定是否有氢气存在.浓硫酸具有吸水性,则装置D的作用是:除去水蒸气;故填:除去水蒸气;
(5)若F中无水硫酸铜白色粉末不变蓝,说明没有氢气;G中的澄清石灰水变浑浊,则可燃气体中一定含有一氧化碳;若F中无水硫酸铜白色粉末变蓝,说明没有氢气,G中的澄清石灰水不变浑浊,说明没有一氧化碳,则可燃气体中一定含有甲烷.
若F中无水硫酸铜白色粉末变蓝,说明有氢气;G中的澄清石灰水变浑浊,说明有一氧化碳,根据表中实验数据,可燃气体的组成可能为氢气和一氧化碳或氢气、一氧化碳和甲烷.故填:一氧化碳;甲烷;2.
点评 本题以实验探究的形式考查常见气体氢气、一氧化碳、二氧化碳和水蒸气的性质,同学们要具有综合的化学知识才能做好此题.

练习册系列答案
相关题目
8.下列叙述正确的是( )
| A. | pH为零的溶液既不显示酸性又不显示碱性 | |
| B. | 打开盛浓硫酸的试剂瓶塞,就可以看到白雾 | |
| C. | 把锌粒投入装有稀硫酸的试管中,试管壁发烫,说明金属与酸的反应是放热反应 | |
| D. | 能使紫色石蕊试液变红的溶液是酸性溶液 |
17.某化学兴趣小组围绕“酸和碱的中和反应”的学习,进行了如下实验.
实验一:5mL氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,可观察到现象为溶液变红,然后加入稀盐酸,用玻璃棒搅拌,溶液褪为无色,有关的反应方程式为HCl+NaOH═NaCl+H2O.
实验二:对实验一反应后溶液中的溶质进行探究.
【提出猜想】
猜想一:只有NaCl
猜想二:有NaCl和NaOH
猜想三:有NaCl和HCl
你认为猜想二不合理,其理由是此时溶液呈无色,而氢氧化钠能使酚酞试液变红.
【设计实验】
【拓展应用】我国土壤的酸碱性有“南酸北碱”之说法,你认为需向酸性土壤中加入熟石灰进行改良.
实验一:5mL氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,可观察到现象为溶液变红,然后加入稀盐酸,用玻璃棒搅拌,溶液褪为无色,有关的反应方程式为HCl+NaOH═NaCl+H2O.
实验二:对实验一反应后溶液中的溶质进行探究.
【提出猜想】
猜想一:只有NaCl
猜想二:有NaCl和NaOH
猜想三:有NaCl和HCl
你认为猜想二不合理,其理由是此时溶液呈无色,而氢氧化钠能使酚酞试液变红.
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入石蕊试液 | 溶液变红 | 猜想三成立 |
4.同学们用高锰酸钾制氧气,制取结束清洗仪器,发现加热高锰酸钾的试管内壁有用水洗刷不掉的黑色固体.
问题一:黑色固体是什么?
【交流讨论】同学们结合实验现象和对高锰酸钾及其分解产物的了解.进行分析判断.
【实验验证】向未洗净的试管中加入某种液体,产生能使带火星木条复燃的气体.证明上述判断正确.加入的液体是过氧化氢溶液.
问题二:用什么洗掉MnO2?
【交流讨论】MnO2与BaCO3、Mg(OH)2、Fe2O3、P2O5、Cu中的某一种物质组成最相近,理由是都是金属氧化物.这种物质能与稀盐酸反应,化学方程式为Fe2O3+6HCl=3H2O+2FeCl3,由此推测MnO2也能与稀盐酸反应.
【实验验证】向未洗净的试管中加入稀盐酸,黑色固体没有变化.
【交流讨论】实验说明同一类物质的化学性质不一定相同.MnO2有什么化学性质,用什么试剂清洗呢?同学们请教老师后决定用草酸(H2C2O4)溶液试一试.
【实验验证】向未洗净的试管中加入草酸溶液,黑色固体果然被除去,同时发现产生许多气泡.
问题三:生产了什么气体?
【交流讨论】化学变化过程中元素不变,因为质量守恒定律,反应物中的元素只有碳、氢、氧,所以产生的气体可能为CO2、CO、H2、O2等.
【实验验证】经检验,产生的气体是CO2,检验CO2气体的操作和现象是:将气体通入澄清石灰水中,石灰水变浑浊,说明该气体是二氧化碳.
【反思提高】以上探究活动中,清除试管内壁附着的难溶物的思路是:先了解其物理性质,尤其是否溶于水,再了解其化学性质,然后选择合适试剂进行清洗.
问题一:黑色固体是什么?
【交流讨论】同学们结合实验现象和对高锰酸钾及其分解产物的了解.进行分析判断.
| 判断 | 依据 |
| 不是KMNO4 | KMNO4能溶于水形成紫红色溶液 |
| 不是K2MnO4(填化学式) | 冲洗试管时出现深绿色溶液,说明该物质能溶于水 |
| 是MnO2 | 其他实验用过MnO2,知道它是不溶于水的黑色固体 |
问题二:用什么洗掉MnO2?
【交流讨论】MnO2与BaCO3、Mg(OH)2、Fe2O3、P2O5、Cu中的某一种物质组成最相近,理由是都是金属氧化物.这种物质能与稀盐酸反应,化学方程式为Fe2O3+6HCl=3H2O+2FeCl3,由此推测MnO2也能与稀盐酸反应.
【实验验证】向未洗净的试管中加入稀盐酸,黑色固体没有变化.
【交流讨论】实验说明同一类物质的化学性质不一定相同.MnO2有什么化学性质,用什么试剂清洗呢?同学们请教老师后决定用草酸(H2C2O4)溶液试一试.
【实验验证】向未洗净的试管中加入草酸溶液,黑色固体果然被除去,同时发现产生许多气泡.
问题三:生产了什么气体?
【交流讨论】化学变化过程中元素不变,因为质量守恒定律,反应物中的元素只有碳、氢、氧,所以产生的气体可能为CO2、CO、H2、O2等.
【实验验证】经检验,产生的气体是CO2,检验CO2气体的操作和现象是:将气体通入澄清石灰水中,石灰水变浑浊,说明该气体是二氧化碳.
【反思提高】以上探究活动中,清除试管内壁附着的难溶物的思路是:先了解其物理性质,尤其是否溶于水,再了解其化学性质,然后选择合适试剂进行清洗.
1.如图所示实验操作中,错误的是( )
| A. | 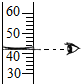 量取液体 | B. | 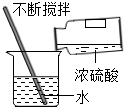 浓硫酸稀释 浓硫酸稀释 | C. |  CO2的验满 | D. |  液体的倾倒 |
19.下列各组物质充分混合,能形成溶液的是( )
| A. | 油与水 | B. | 清洁剂与水 | C. | 碘与酒精 | D. | 二氧化猛与水 |
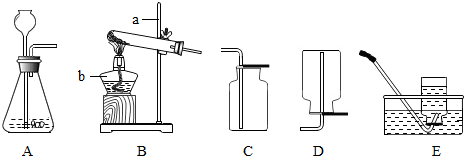
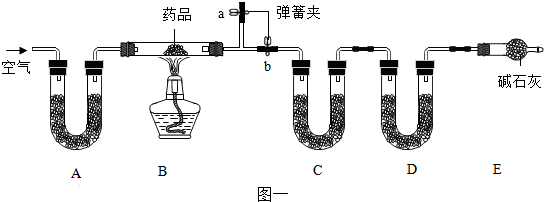

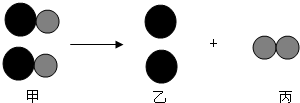
 ”和“
”和“ ”分别表示不同质子数的原子在化学变化前后的微观模拟示意图下.请回答下列问题:
”分别表示不同质子数的原子在化学变化前后的微观模拟示意图下.请回答下列问题: