题目内容
3.某化工厂排出的废水透明、澄清、略显蓝色.一同学取少量废水,用盐酸酸化,有白色沉淀生成(不溶于稀硝酸).过滤,将所得的滤液分成两份,一份滤液中加入稀硫酸,也有白色沉淀生成(不溶于稀硝酸);另一份滤液中加入足量NaOH溶液,产生蓝色沉淀.试回答:(1)过滤后,向滤液中滴加NaOH溶液,开始时观察不到蓝色沉淀,原因是:盐酸过量.
(2)该同学设计了一个从废水中除去重金属离子的实验[已知白色的Fe(OH)2固体在潮湿的空气中可生成红褐色的Fe(OH)3],方案如下:
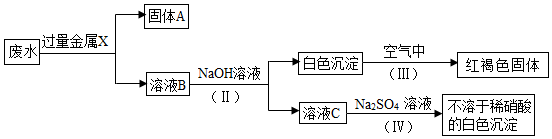
①固体A中一定含有的物质为Fe、Ag和Cu(写化学式).
②B溶液中的溶质一定含有Fe(NO3)2、Ba(NO3)2(写化学式).
分析 根据题中的框图可知:已知红褐色固体是氢氧化铁,所以白色沉淀是氢氧化亚铁,取废水,加盐酸酸化,会生成不溶于稀硝酸的白色沉淀,所以溶液中含有硝酸银,所得的滤液分成两份,一份滤液中加入稀硫酸,也有白色沉淀生成(沉淀不溶于稀硝酸),所以溶液中含有硝酸钡,另一份滤液中加入足量NaOH溶液,产生蓝色沉淀,所以溶液中含有硝酸铜,通过分析可知,X是金属铁,铁把银、铜置换出来,所以固体A为Ag、Cu、Fe;又由于加入过量的铁和出现的白色沉淀,所以B溶液中一定有Fe (NO3)2和Ba (NO3)2,然后将推出的物质进行验证即可.
解答 解:由题中的框图可知:已知红褐色固体是氢氧化铁,所以白色沉淀是氢氧化亚铁,取废水,加盐酸酸化,会生成不溶于稀硝酸的白色沉淀,所以溶液中含有硝酸银,所得的滤液分成两份,一份滤液中加入稀硫酸,也有白色沉淀生成(沉淀不溶于稀硝酸),所以溶液中含有硝酸钡,另一份滤液中加入足量NaOH溶液,产生蓝色沉淀,所以溶液中含有硝酸铜,通过分析可知,X是金属铁,铁把银、铜置换出来,所以固体A为Ag、Cu、Fe;又由于加入过量的铁和出现的白色沉淀,所以B溶液中一定有Fe (NO3)2和Ba (NO3)2,所以
(1)过滤后,向滤液中滴加NaOH溶液,开始时观察不到蓝色沉淀,原因是:盐酸过量;
(2)①固体A中一定含有的物质为:Fe、Ag和Cu;
②B溶液中的溶质一定含有:Fe(NO3)2、Ba(NO3)2.
故答案为:(1)盐酸过量;
(2)①Fe、Ag和Cu;
②Fe(NO3)2、Ba(NO3)2.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
13.缺乏维生素A(化学式为C20H30O),会引起夜盲证.下列说法正确的是( )
| A. | 维生素A的相对分子质量286g | |
| B. | 维生素A中碳、氢、氧元素的质量比为20:30:1 | |
| C. | 维生素A中碳元素的质量分数是83.9% | |
| D. | 维生素A是由20个碳原子、30个氢原子、1个氧原子构成的 |
11.第16届广州亚运会将于2010年11月12日在我国广州开幕,届时可能会用到大型遥控飞艇作为宣传工具以渲染活动气氛.为了飞艇在空中飞行安全而有效,根据下表中气体的性质,最适合填充飞艇的气体是氦气.
| 气 体 | 氢 气 | 氦 气 | 氮 气 | 空 气 | 氧 气 | |
| 性质 | 密 度/kg•m-3 | 0.09 | 0.18 | 1.25 | 1.29 | 1.43 |
| 可 燃 性 | 可 燃 | 不可燃 | 不可燃 | 不可燃 | 不可燃 | |
18.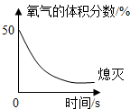 足量蜡烛(由碳、氢元素组成)在密闭集气瓶内(起始时常压)燃烧至熄灭,瓶内氧气体积分数随时间变化如图所示.下列说法正确的是( )
足量蜡烛(由碳、氢元素组成)在密闭集气瓶内(起始时常压)燃烧至熄灭,瓶内氧气体积分数随时间变化如图所示.下列说法正确的是( )
①起始阶段蜡烛燃烧比在空气中燃烧剧烈
②燃烧过程中,瓶内物质总质量不变
③蜡烛熄灭是由于瓶内氧气浓度过低
④若产物中二氧化碳与水分子个数相等,则反应后瓶内气体总质量增加.
 足量蜡烛(由碳、氢元素组成)在密闭集气瓶内(起始时常压)燃烧至熄灭,瓶内氧气体积分数随时间变化如图所示.下列说法正确的是( )
足量蜡烛(由碳、氢元素组成)在密闭集气瓶内(起始时常压)燃烧至熄灭,瓶内氧气体积分数随时间变化如图所示.下列说法正确的是( )①起始阶段蜡烛燃烧比在空气中燃烧剧烈
②燃烧过程中,瓶内物质总质量不变
③蜡烛熄灭是由于瓶内氧气浓度过低
④若产物中二氧化碳与水分子个数相等,则反应后瓶内气体总质量增加.
| A. | ③④ | B. | ①②③ | C. | ①②④ | D. | ①②③④ |
8.下列说法错误的是( )
| A. | 氧气很活泼,常温时可以和所有金属反应 | |
| B. | 铁生锈、食物腐烂、呼吸作用都属于缓慢氧化 | |
| C. | 高炉炼铁时CO是作为还原剂 | |
| D. | 泡沫CO2可灭火的主要原因是不支持燃烧,使可燃物和空气隔绝 |
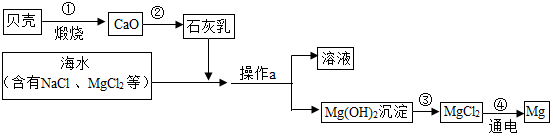
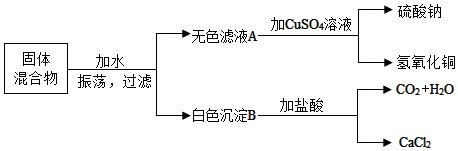
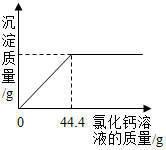 超市卖的纯碱产品中往往含有少量的氯化钠,某化学兴趣小组的同学通过实验来测定某品牌的纯碱样品中碳酸钠的质量分数.他们取了5g该纯碱样品,在烧杯中配制成60g溶液,再向其中逐滴加入10%的氯化钙溶液,测得加入氯化钙的质量与产生沉淀的质量关系如图所示.请回答下列问题:
超市卖的纯碱产品中往往含有少量的氯化钠,某化学兴趣小组的同学通过实验来测定某品牌的纯碱样品中碳酸钠的质量分数.他们取了5g该纯碱样品,在烧杯中配制成60g溶液,再向其中逐滴加入10%的氯化钙溶液,测得加入氯化钙的质量与产生沉淀的质量关系如图所示.请回答下列问题: