题目内容
14.海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钾等.综合利用海水制备金属镁的流程如图所示: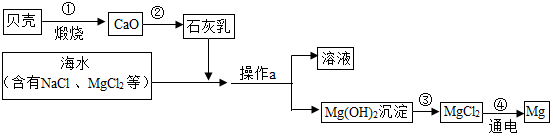
〔1〕贝壳主要成分的化学式是CaCO3;
〔2〕操作a的名称是过滤;
〔3〕写出第②步反应的化学方程式CaO+H2O═Ca(OH)2;
〔4〕在第③步化学反应中所加的试剂是HCl(填化学式)
〔5〕请写出第④步化学反应方程式MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.
分析 根据已有的知识进行分析,贝壳的主要成分是碳酸钙,过滤时分离不溶性固体和液体的方法,该实验操作中使用的玻璃仪器有烧杯、漏斗和玻璃棒,氧化钙能与水反应生成氢氧化钙,氢氧化镁能和盐酸反应生成氯化镁和水.
解答 解:(1)贝壳的主要成分是碳酸钙,故填:CaCO3;
(2)经过操作a得到了溶液和氢氧化镁的沉淀,该操作时分离的不溶性固体和液体,是过滤操作,故填:过滤;
(3)氧化钙能与水反应生成氢氧化钙,化学方程式为:CaO+H2O═Ca(OH)2;故填:CaO+H2O═Ca(OH)2;
(4)氢氧化镁能和盐酸反应生成氯化镁和水,故填:HCl.
(5)电解MgCl2生成金属镁和氯气,反应化学方程式为:MgCl2 $\frac{\underline{\;通电\;}}{\;}$ Mg+Cl2↑;故填:MgCl2 $\frac{\underline{\;通电\;}}{\;}$ Mg+Cl2↑.
点评 本题考查了从海水中提取镁的原理和方法,从氯化镁中提取镁单质,应电解熔融态的氯化镁,而不能用置换的方法得到镁.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.在中学所学的化学反应中,有很多反应没有明显现象.某探究小组想通过实验来证明CO2与NaOH溶液反应确实发生了,他们做了以下探究过程.
【查阅资料】通常状况下,1体积水能溶解1体积二氧化碳.
【设计实验】甲同学设计了三个实验进行验证,请你帮他完成下列实验报告.
密封线内不得答题
【反思交流】
(1)实验①由于甲同学选用的仪器不当,导致未能观察到明显现象,乙同学将甲同学的广口瓶替换成塑料瓶,看到了塑料瓶变瘪现象,证明CO2可以与NaOH溶液反应.丙同学认为乙同学的改进实验仍然存在缺陷,应增加一个对比实验,证明CO2确实可以与NaOH溶液发生反应,该对比实验所用的试剂是水和二氧化碳 .
(2)请判断③中V>200mL(填“>”、“<”或“=”),理由是如果没有NaOH溶液,V≤200mL时CO2能够完全溶于水也会产生同样现象.
【实验结论】通过实验探究,证明了氢氧化钠溶液可以与二氧化碳反应.
【查阅资料】通常状况下,1体积水能溶解1体积二氧化碳.
【设计实验】甲同学设计了三个实验进行验证,请你帮他完成下列实验报告.
| 实验操作 | 实验现象 | 实验结论及解释 | |
| ① |  | 氢氧化钠溶液可以与CO2反应, 反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O | |
| ② |  | 气球膨胀 | 氢氧化钠溶液可以与CO2反应. |
| ③ |  洗气瓶中的溶液为氢氧化钠溶液或澄清石灰水(均为200mL) | A,B均无明显变化 | 氢氧化钠溶液可以与CO2反应. B中盛放的溶液是澄清石灰水. |
【反思交流】
(1)实验①由于甲同学选用的仪器不当,导致未能观察到明显现象,乙同学将甲同学的广口瓶替换成塑料瓶,看到了塑料瓶变瘪现象,证明CO2可以与NaOH溶液反应.丙同学认为乙同学的改进实验仍然存在缺陷,应增加一个对比实验,证明CO2确实可以与NaOH溶液发生反应,该对比实验所用的试剂是水和二氧化碳 .
(2)请判断③中V>200mL(填“>”、“<”或“=”),理由是如果没有NaOH溶液,V≤200mL时CO2能够完全溶于水也会产生同样现象.
【实验结论】通过实验探究,证明了氢氧化钠溶液可以与二氧化碳反应.
5. 人吸入空气,排出CO2等气体.为了证明人呼出的气体中含有CO2且能有效排除空气中CO2的干扰,某学生设计了下图所示的实验装置,为了除去空气中的CO2和检验人呼出的气体中含有CO2,则锥形瓶Ⅰ、Ⅱ中加入的试剂为( )
人吸入空气,排出CO2等气体.为了证明人呼出的气体中含有CO2且能有效排除空气中CO2的干扰,某学生设计了下图所示的实验装置,为了除去空气中的CO2和检验人呼出的气体中含有CO2,则锥形瓶Ⅰ、Ⅱ中加入的试剂为( )
 人吸入空气,排出CO2等气体.为了证明人呼出的气体中含有CO2且能有效排除空气中CO2的干扰,某学生设计了下图所示的实验装置,为了除去空气中的CO2和检验人呼出的气体中含有CO2,则锥形瓶Ⅰ、Ⅱ中加入的试剂为( )
人吸入空气,排出CO2等气体.为了证明人呼出的气体中含有CO2且能有效排除空气中CO2的干扰,某学生设计了下图所示的实验装置,为了除去空气中的CO2和检验人呼出的气体中含有CO2,则锥形瓶Ⅰ、Ⅱ中加入的试剂为( ) | 瓶I | 瓶Ⅱ | |
| A | Ca(OH)2 | NaOH |
| B | NaOH | Ca(OH)2 |
| C | 石蕊 | 酚酞 |
| D | Na2SO4 | CaCl2 |
| A. | A | B. | B | C. | C | D. | D |
2. 在分别盛有甲、乙两种固体的A、B试管中加入等量的水充分振荡,在20℃时,甲中还有一部分没有溶解,乙中完全溶解.下列有关所得溶液的说法正确的是( )
在分别盛有甲、乙两种固体的A、B试管中加入等量的水充分振荡,在20℃时,甲中还有一部分没有溶解,乙中完全溶解.下列有关所得溶液的说法正确的是( )
 在分别盛有甲、乙两种固体的A、B试管中加入等量的水充分振荡,在20℃时,甲中还有一部分没有溶解,乙中完全溶解.下列有关所得溶液的说法正确的是( )
在分别盛有甲、乙两种固体的A、B试管中加入等量的水充分振荡,在20℃时,甲中还有一部分没有溶解,乙中完全溶解.下列有关所得溶液的说法正确的是( )| A. | 20℃时,甲溶液一定是饱和溶液 | |
| B. | 20℃时,乙溶液一定是饱和溶液 | |
| C. | 20℃时,两种溶液可能均为不饱和溶液 | |
| D. | 20℃时,乙在水中的溶解能力一定比甲强 |
9.多数食品易吸收空气中的水分变潮,并与空气中的O2 反应腐败.生产上多在食品上放入一包CaO粉未,使食品保持干燥.现已研究成功在食品中放入一包铁粉(包裹在多孔泡沫中)铁粉吸收水分和氧气变成铁锈,从而保护食品.下列说法不正确的( )
| A. | 两干燥剂袋上都要有明显的“勿食”字样 | |
| B. | 生成铁锈的主要成分是氧化铁 | |
| C. | 铁粉干燥剂能与水和O2 发生化学反应 | |
| D. | CaO干燥剂保护食品的效果比铁粉干燥剂好 |
 根据右图所示的溶解度曲线图,回答问题:
根据右图所示的溶解度曲线图,回答问题: