题目内容
5.如图表示某些物质间转化关系,A、D是由相同元素组成的固体,且A为紫黑色,C为黑色粉末,B、E为常见气体,X与F是由相同元素组成的无色液体,且X具有消毒杀菌作用,Y是一种红色金属.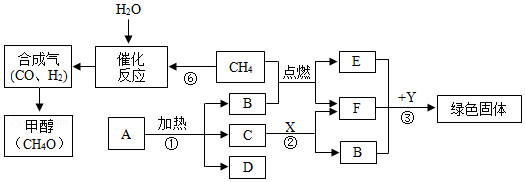
(1)X的化学式是H2O2;
(2)C物质在反应②中的作用催化作用;
(3)写出反应方程式:①2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑;③2Cu+O2+H2O+CO2═Cu2(OH)2CO3;
(4)理论上合成气中CO和H2的分子个数比为1:2.“合成气”合成甲醇时,反应中CO、H2的质量比为7:1.
分析 在做推断题时,首先找到这一题的题眼,然后根据题眼推断出其它物质.这一题的题眼是甲烷可在B中燃烧,所以可推断B为氧气.
解答 解:因甲烷可在B中燃烧,所以B为氧气,而B又是紫黑色A加热得到,所以可断定A为高锰酸钾,又知X与F是由相同元素组成的无色液体,且X具有消毒杀菌作用,所以X为双氧水,C为二氧化锰,F为水,D是锰酸钾;又因Y是一种红色金属,且E、F、B和Y生成绿色物质,所以Y为铜,而绿色物质为铜绿.带入框图,推断合理;
由题可知合成气体是CO和H2组成,由两气体按分子数之比为1:2进行化合,可以产生CH4O.
(1)X是过氧化氢,故填:H2O2;
(2)C是二氧化锰,在反应②中做的是催化剂,起催化作用,故填:催化作用;
(3)①是高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑;
③是铜、氧气和二氧化碳以及水反应生成碱式碳酸铜,故填:2Cu+O2+H2O+CO2═Cu2(OH)2CO3;
(4)合成气体是CO和H2组成,能生成CH4O,由两气体按分子数之比为1:2进行化合,二者的质量比为28:4=7:1,故填:1:2;7:1.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.

练习册系列答案
相关题目
15.学习了有关金属的性质,同学们对影响化学反应速率的因素进行探究.
(1)发现和提出问题:
①镁在空气中就能够剧烈燃烧,铁丝在氧气中才能够剧烈燃烧,此现象说明镁比铁活泼,化学反应的速率与金属本身的性质有关.
②夏天,将食品放在冰箱里不容易变质,这一事例说明温度也能影响化学反应速率.温度如何影响反应速率呢?
(2)猜想与假设:其它条件相同时,温度越高,反应速率越快.
(3)收集证据
取10mL稀硫酸,均分为两等份,分别放入试管中,各加入大小相同的锌粒,再分别放入盛有20℃和80℃水的烧杯中,塞紧带有气球的瓶塞,观察现象.
(1)发现和提出问题:
①镁在空气中就能够剧烈燃烧,铁丝在氧气中才能够剧烈燃烧,此现象说明镁比铁活泼,化学反应的速率与金属本身的性质有关.
②夏天,将食品放在冰箱里不容易变质,这一事例说明温度也能影响化学反应速率.温度如何影响反应速率呢?
(2)猜想与假设:其它条件相同时,温度越高,反应速率越快.
(3)收集证据
取10mL稀硫酸,均分为两等份,分别放入试管中,各加入大小相同的锌粒,再分别放入盛有20℃和80℃水的烧杯中,塞紧带有气球的瓶塞,观察现象.
| 实验步骤 | 实验现象 | 实验结论 |
 | a、b中均有气泡产生,b中产生气泡的速度比a快(或b中气球膨胀的速度比a快) | 其它条件下相同时,温度越高,反应速率越快.反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑ |
13.把一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的量如下表.下列说法正确的是( )
A.X=2.0,乙一定是催化剂 B.反应的基本类型为化合反应
C.参加反应的甲、丙质量比是1:2 D.反应物为甲、丙.
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量(g) | 4.0 | 2.0 | 3.0 | 2.0 |
| 反应后的质量(g) | 1.2 | X | 2.4 | 5.4 |
C.参加反应的甲、丙质量比是1:2 D.反应物为甲、丙.
17.实验室中用过氧化氢、氯酸钾、高锰酸钾都可以制取氧气,其原因是( )
| A. | 都含有氧元素 | B. | 都含有氧气 | C. | 都含有氧分子 | D. | 都属于氧化物 |
14.水是重要的自然资源,下列说法正确的是( )
| A. | 矿泉水是纯净物 | |
| B. | 保持水的化学性质的最小粒子是氧分子 | |
| C. | 水变成水蒸气,分子间隔增大 | |
| D. | 水由氢气和氧气组成 |
15.除去二氧化碳中混有的少量一氧化碳,可以将混合气体( )
| A. | 点燃 | B. | 通过足量水 | ||
| C. | 通过足量澄清石灰水 | D. | 通过足量灼热的氧化铜 |
 某同学利用如图用品进行二氧化碳性质实验.【实验1】向图1集满CO2的软塑料瓶中,迅速倒入半瓶蒸馏水,旋紧瓶盖.充分振荡,观察到塑料瓶变瘪,原因是二氧化碳溶于水或与水反应,导致气体减少,瓶内压强减小.
某同学利用如图用品进行二氧化碳性质实验.【实验1】向图1集满CO2的软塑料瓶中,迅速倒入半瓶蒸馏水,旋紧瓶盖.充分振荡,观察到塑料瓶变瘪,原因是二氧化碳溶于水或与水反应,导致气体减少,瓶内压强减小.