题目内容
15.学习了有关金属的性质,同学们对影响化学反应速率的因素进行探究.(1)发现和提出问题:
①镁在空气中就能够剧烈燃烧,铁丝在氧气中才能够剧烈燃烧,此现象说明镁比铁活泼,化学反应的速率与金属本身的性质有关.
②夏天,将食品放在冰箱里不容易变质,这一事例说明温度也能影响化学反应速率.温度如何影响反应速率呢?
(2)猜想与假设:其它条件相同时,温度越高,反应速率越快.
(3)收集证据
取10mL稀硫酸,均分为两等份,分别放入试管中,各加入大小相同的锌粒,再分别放入盛有20℃和80℃水的烧杯中,塞紧带有气球的瓶塞,观察现象.
| 实验步骤 | 实验现象 | 实验结论 |
 | a、b中均有气泡产生,b中产生气泡的速度比a快(或b中气球膨胀的速度比a快) | 其它条件下相同时,温度越高,反应速率越快.反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑ |
分析 (1)根据金属的活动性来分析;
(2)根据实验的结论来分析所能观察到的实验现象,根据化学反应的原理来书写化学方程式.
解答 解:(1)①在金属活动顺序中,镁排在铁的前面,这说明镁比铁活泼,所以镁在空气中就能够剧烈燃烧,铁丝在氧气中才能够剧烈燃烧,故填:镁比铁活泼;
(3)因为其它条件下相同时,温度越高,反应速率越快,所以当取10mL稀硫酸,均分为两等份,分别放入试管中,各加入大小相同的锌粒,再分别放入盛有20℃和80℃水的烧杯中,塞紧带有气球的瓶塞,会观察到a、b中均有气泡产生,b中产生气泡的速度比a快(或b中气球膨胀的速度比a快);锌与硫酸反应生成硫酸锌和氢气;故填:实验现象:a、b中均有气泡产生,b中产生气泡的速度比a快(或b中气球膨胀的速度比a快);实验结论:Zn+H2SO4=ZnSO4+H2↑.
点评 本题通过实验探究了影响化学反应速率的因素,难度不大.

练习册系列答案
相关题目
5.下列有关$\frac{1}{3}$的说法中不正确的是( )
| A. | 用试管给液体加热时,液体量不超过试管容积的$\frac{1}{3}$ | |
| B. | 用试管给液体加热时,试管夹夹在离管口约$\frac{1}{3}$处 | |
| C. | 空气中氧气约占总体积的$\frac{1}{3}$ | |
| D. | 用蒸发皿给液体加热时,液体量不超过蒸发皿容积的$\frac{1}{3}$ |
6.某气体易溶于水,密度比空气的密度小,在实验室中可以用两种固体药品混合后加热制取该气体.若将制取这种气体与用高锰酸钾制取氧气相比较,下列说法中正确的是( )
| A. | 这种气体与氧气都可以用排水法收集 | |
| B. | 这种气体与氧气都可以用向上排空气法收集 | |
| C. | 这种气体与氧气可以用相同的气体发生装置来制取 | |
| D. | 收集这种气体的方法不可以用来收集氧气 | |
| E. | 制取这种气体的发生装置不可以用来制取氧气 |
3.下列关于氧气的说法正确的是( )
| A. | 氧气在空气中的体积分数为78% | |
| B. | 液态氧可用作火箭的助燃剂 | |
| C. | 硫在氧气中燃烧发出黄色火焰 | |
| D. | 鱼类能在水中生存,证明氧气易溶于水 |
20.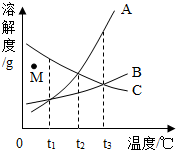 如图为A、B、C三种固体物质的溶解度曲线图(A、B、C析出晶体时均不含结晶水),根据曲线图所示,下列说法正确的是( )
如图为A、B、C三种固体物质的溶解度曲线图(A、B、C析出晶体时均不含结晶水),根据曲线图所示,下列说法正确的是( )
 如图为A、B、C三种固体物质的溶解度曲线图(A、B、C析出晶体时均不含结晶水),根据曲线图所示,下列说法正确的是( )
如图为A、B、C三种固体物质的溶解度曲线图(A、B、C析出晶体时均不含结晶水),根据曲线图所示,下列说法正确的是( )| A. | t2℃时,溶解度最大的物质是A | |
| B. | 若将M点处C的不饱和溶液变为饱和溶液,可以选择的方法是降低温度 | |
| C. | t2℃时,将等质量的A、B、C的饱和溶液都升温到t3℃,溶液中溶剂质量的大小关系是(忽略水的挥发)B>A=C | |
| D. | t1℃时,将A、B、C三种固体物质分别溶于水所得溶液的溶质质量分数C>A=B |
7.学习了二氧化锰对过氧化氢分解有催化作用的知识后,某兴趣小组同学在课外进行了有关过氧化氢分解反应的再探究.
【探究一】影响过氧化氢分解速率的因素有哪些?
兴趣小组同学做了四个实验,实验数据如表:
(1)过氧化氢分解速率与温度的关系是其他条件相同时,温度升高,过氧化氢分解速率加快.
(2)能说明过氧化氢的分解速率与其质量分数有关的实验是①②(填实验序号).
【探究二】MnO2的聚集状态是否影响其催化效果?
将质量相同但聚集状态不同的MnO2分别加入到5mL5%的H2O2溶液中,测试结果如下:
由上述实验得到的结论是粉末状二氧化锰比块状二氧化锰催化效果要好.
【探究三】其他金属氧化物能否起到类似MnO2的催化作用?
兴趣小组同学用天平称量0.2g CuO,用量筒量取5mL 5% 的H2O2溶液,进行如下图所示实验(①~⑦代表实验操作步骤).

(1)小组同学通过上述实验得出结论:CuO可作过氧化氢分解的催化剂,支持该结论的实验证据是①不复燃,③复燃;⑥固体质量为0.2g;⑦溶液中有气泡放出,带火星的木条复燃.
(2)过氧化氢能被CuO催化分解放出氧气的化学反应方程式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
(3)欲比较不同催化剂CuO和MnO2对H2O2分解速率的影响,实验时需要控制的变量有温度、H2O2溶液溶质质量分数及体积、CuO和MnO2的质量及聚集状态.
【探究一】影响过氧化氢分解速率的因素有哪些?
兴趣小组同学做了四个实验,实验数据如表:
| 实验 序号 | H2O2溶液的溶质质量分数% | H2O2溶液的体积/mL | 温度/℃ | MnO2的用量/g | 收集O2的体积/mL | 反应 时间 |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16s |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6s |
| ③ | 30 | 5 | 35 | 0 | 4 | 98min |
| ④ | 30 | 5 | 55 | 0 | 4 | 2 0min |
(2)能说明过氧化氢的分解速率与其质量分数有关的实验是①②(填实验序号).
【探究二】MnO2的聚集状态是否影响其催化效果?
将质量相同但聚集状态不同的MnO2分别加入到5mL5%的H2O2溶液中,测试结果如下:
| MnO2的状态 | 操作情况 | 观察结果 |
| 粉末状 | 混合不振荡 | 剧烈反应,带火星的木条复燃 |
| 块状 | 反应较慢,火星红亮但木条未复燃 |
【探究三】其他金属氧化物能否起到类似MnO2的催化作用?
兴趣小组同学用天平称量0.2g CuO,用量筒量取5mL 5% 的H2O2溶液,进行如下图所示实验(①~⑦代表实验操作步骤).

(1)小组同学通过上述实验得出结论:CuO可作过氧化氢分解的催化剂,支持该结论的实验证据是①不复燃,③复燃;⑥固体质量为0.2g;⑦溶液中有气泡放出,带火星的木条复燃.
(2)过氧化氢能被CuO催化分解放出氧气的化学反应方程式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
(3)欲比较不同催化剂CuO和MnO2对H2O2分解速率的影响,实验时需要控制的变量有温度、H2O2溶液溶质质量分数及体积、CuO和MnO2的质量及聚集状态.
4.“分子机器”是指在分子尺寸上制造的一类分子器件,其长短仅相当于1纳米左右(1纳米=10-9米),它的驱动方式是通过外部刺激(如电能、光照等)使分子结构发生改变,从而对外做功.下列关于分子机器的说法中,正确的是( )
| A. | 肉眼能直接观察到分子机器 | |
| B. | 分子机器驱动过程中,发生了化学变化 | |
| C. | 分子机器的驱动不需要能量 | |
| D. | 分子机器“发动机”驱动方式与普通发动机相同 |