题目内容
18.某同学需测定某100g过氧化氢溶液中所含过氧化氢的质量.他取10g二氧化锰放入烧杯中,并将该过氧化氢溶液全部加入,不同时间用电子天平测量其质量,所得读数如表所示:| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 烧杯及所盛物质总质量/g | 335.70 | 334.30 | 334.00 | 333.50 | 333.00 | 332.50 | 332.50 |
(2)计算100g过氧化氢溶液中过氧化氢质量分数为多少?(写出计算过程)
分析 (1)根据质量守恒定律,反应前即时间为0时烧杯及所盛物质总质量与完全反应后即不再产生气体时间为5min时烧杯及所盛物质总质量的差,即为反应放出气体氧气的质量;
(2)根据过氧化氢在二氧化锰催化下分解生成水和氧气的化学方程式,由生成氧气的质量计算出反应消耗过氧化氢的质量,即100g溶液中所含溶质的质量;利用所计算溶质过氧化氢的质量与溶液的质量100g运用溶质质量分数计算公式进行计算即可,计算出所用溶液中溶质的质量分数.
解答 解:(1)取10g二氧化锰放入烧杯中加入足量100g过氧化氢溶液,待不再放出气体时,烧杯及所剩余物质的总质量为332.50g,反应前后的质量差即为放出氧气的质量,反应生成氧气质量为:335.70g-332.50g=3.2g;
(2)设过氧化氢的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 3.2g
$\frac{68}{x}$=$\frac{32}{3.2g}$
x=6.8g
过氧化氢溶液的质量分数为:$\frac{6.8g}{100g}$×100%=6.8%.
故答案为:(1)3.2g;
(2)过氧化氢溶液的溶质质量分数为6.8%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
8.在探究CO2与NaOH溶液反应的实验时,小丫向装有CO2气体的铝制易拉罐中,加入一定量的NaOH浓溶液,立即将易拉罐口封闭(不漏气),轻轻摇动易拉罐,发现易拉罐很快变瘪,但过一段时间后,易拉罐又重新鼓起来(反应过程中温度的变化忽略不计).
[讨论]根据易拉罐变瘪现象,小丫认为CO2能与NaOH溶液反应,但小龙认为不足以得出此结论,需补充下列实验.
[结论]CO2与NaOH反应的化学方程式是2NaOH+CO2═Na2CO3+H2O.
[提出问题]易拉罐为什么又重新鼓起来?是不是反应又产生了气体,该气体的成分是什么?
[查阅资料]①Na2CO3具有较强的热稳定性,只有在高温条件下才会分解;
②铝不仅与酸反应,还能与碱溶液反应2Al+2NaOH+2H2O═2X+3H2↑,X的化学式为NaAlO2.
[实验验证]①将易拉罐口打开,迅速用燃着的木条伸入罐口,发出“噗”的一声,产生淡蓝色火焰,片刻后熄灭.结论:该过程产生的是H2.
②取少量铝片于试管中,先加入适量的水,无明显变化.片刻后再加入少量的氢氧化钠浓溶液,产生气泡.该步实验的目的是对比.
[讨论]根据易拉罐变瘪现象,小丫认为CO2能与NaOH溶液反应,但小龙认为不足以得出此结论,需补充下列实验.
| 实验操作 | 现象 | 结论 |
| 取罐中的溶液少量放入试管中,再滴加足量稀盐酸,观察现象 | 产生气泡 | 证明CO2与NaOH溶液混合有新物质生成 |
[提出问题]易拉罐为什么又重新鼓起来?是不是反应又产生了气体,该气体的成分是什么?
[查阅资料]①Na2CO3具有较强的热稳定性,只有在高温条件下才会分解;
②铝不仅与酸反应,还能与碱溶液反应2Al+2NaOH+2H2O═2X+3H2↑,X的化学式为NaAlO2.
[实验验证]①将易拉罐口打开,迅速用燃着的木条伸入罐口,发出“噗”的一声,产生淡蓝色火焰,片刻后熄灭.结论:该过程产生的是H2.
②取少量铝片于试管中,先加入适量的水,无明显变化.片刻后再加入少量的氢氧化钠浓溶液,产生气泡.该步实验的目的是对比.
9.把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如表所示:
下列说法正确的是( )
| 物 质 | A | B | C | D |
| 反应前质量/g | 19.7 | 8.7 | 21.6 | 0.4 |
| 反应后质量/g | 待测 | 17.4 | 0 | 3.6 |
| A. | 若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为2:1 | |
| B. | 反应后密闭容器中A的质量为19.7 g | |
| C. | 反应过程中,物质B和物质D变化的质量比为87:36 | |
| D. | 物质C一定是化合物,物质D可能是单质 |
6.二氧化锰可以用来催化过氧化氢的分解:现将0.5g MnO2加入50mL过氧化氢溶液中,收集产生的氧气(该实验条件下,氧气的密度是1.33g/L),每20s 记录所收集的气体体积并记录在表中:
(*平均反应速率是指每20秒内气体产生的平均速率)
(1)上述表格中①代表的数据是0.6
(2)如果重做以上实验,并用1.0g MnO2做催化剂,最终产生的氧气总量会如何变化?不变(填“增大”、“减少”或“不变”)理由是二氧化锰能够改变过氧化氢的分解速率,而与最终产生氧气的总质量无关,两次过氧化氢质量相等,因此产生氧气质量相等
(3)该实验条件下,最终产生的氧气质量是0.12克.(结果保留两位小数)
| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
| 氧气体积/cm3 | 0 | 48 | 70 | 82 | 88 | 88 |
| 平均反应速率/cm3 s-1 | 0.0 | 2.4 | 1.1 | ① 0.6 | 0.3 | 0.0 |
(1)上述表格中①代表的数据是0.6
(2)如果重做以上实验,并用1.0g MnO2做催化剂,最终产生的氧气总量会如何变化?不变(填“增大”、“减少”或“不变”)理由是二氧化锰能够改变过氧化氢的分解速率,而与最终产生氧气的总质量无关,两次过氧化氢质量相等,因此产生氧气质量相等
(3)该实验条件下,最终产生的氧气质量是0.12克.(结果保留两位小数)
13.以下哪个过程能正确地表示工业中大规模生产氧气的过程( )
| A. | 空气$\stackrel{液化}{→}$液态空气$\stackrel{分离}{→}$氧气 | |
| B. | 二氧化碳$\stackrel{绿色植物}{→}$氧气 | |
| C. | 高锰酸钾(KMnO4)$\stackrel{加热}{→}$锰酸钾(K2MnO4)+二氧化锰(MnO2)+氧气(O2) | |
| D. | 过氧化氢(H2O2)$\stackrel{二氧化锰}{→}$水(H2O)+氧气(O2) |
3.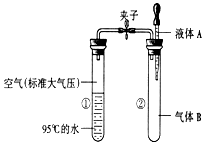 如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合可能是下列的( )
如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合可能是下列的( )
 如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合可能是下列的( )
如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了.则液体A和气体B的组合可能是下列的( )| A. | 氢氧化钙溶液、一氧化碳 | B. | 硝酸银、氯化氢 | ||
| C. | 酒精、氧气 | D. | 水、甲烷 |
7.2005年在某些国家和我国一些地区的有些食品中发现了对人体有害的苏丹红I号.对苏丹红I号(化学式为C16H12N2O)的叙述,不正确的是( )
| A. | 是一种有机化合物 | |
| B. | 由四种元素组成 | |
| C. | 每个分子中含有31个原子 | |
| D. | 在这种物质中碳、氧两种元素质量比为16:1 |
 为测定空气中氧气的含量,某同学设计如下方案:选用实际容积为40mL的试管作反应容器,将过量的白磷放入试管,用橡皮塞塞紧试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成实验装置,活塞前沿稳定在20mL刻度处(如图所示).假设此实验能够按照该同学的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:
为测定空气中氧气的含量,某同学设计如下方案:选用实际容积为40mL的试管作反应容器,将过量的白磷放入试管,用橡皮塞塞紧试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成实验装置,活塞前沿稳定在20mL刻度处(如图所示).假设此实验能够按照该同学的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题: