题目内容
3.某氯化钠样品中含有硝酸钠杂质,学校化学兴趣小组的同学开展了测定其中NaCl质量分数的探究实验,他们设计了如图的实验方案: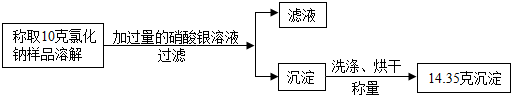
(1)过滤中使用到玻璃棒的作用是引流;
(2)沉淀应该洗涤后烘干称量,否则会使测定的结果偏大(填“偏大”可“偏小”);
(3)该样品中氯化钠的质量分数是多少?(写出解题过程)
分析 根据过滤操作中玻璃棒的作用解答,根据沉淀质量偏大则计算结果偏大解答,根据反应的化学方程式结合题干提供的数据进行计算即可.
解答 解:(1)过滤中使用玻璃棒的作用是引流,故填:引流;
(2)沉淀应该洗涤后烘干称量,如果不烘干则会使沉淀的质量变大,测定的结果变大,故填:偏大;
(3)设氯化钠的质量为x
NaCl+AgNO3=AgCl↓+NaNO3
58.5 143.5
x 14.35g
$\frac{58.5}{143.5}=\frac{x}{14.35g}$ x=5.85g
样品中氯化钠的质量分数=$\frac{5.85g}{10g}×100%$=58.5%
答:样品中氯化钠的质量分数为58.5%.
点评 本题考查的是根据化学方程式的计算,解答本题的关键是掌握实验操作的注意事项以及熟练掌握反应的化学方程式.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
12.相等质量的下列物质,在氧气中完全燃烧,消耗氧气最多的是( )
| A. | 镁 | B. | 碳 | C. | 磷 | D. | 铁 |
10.下列物质的名称、化学式、分类均正确的是( )
| A. | 硫酸钠 NaSO4 盐 | B. | 氧化钙 CaO 氧化物 | ||
| C. | 烧碱 KOH 碱 | D. | 甲烷 CH4 无机物 |
17.化学帮助我们认识和改造物质世界,材料的开发和研制为我们的生活增加了丰富的色彩.以下物质属于有机合成材料的是( )
| A. | 羊毛纤维 | B. | 合金 | C. | 玻璃纤维 | D. | 塑料 |
8.通过查阅资料得知:将熟石灰与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.为了制取氢氧化钾,兴趣小组的同学将少量熟石灰放入烧杯中,再向其中加入一定量碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示,请你与小组同学共同完成以下探究:
【提出问题1】固体A中的成分是什么?
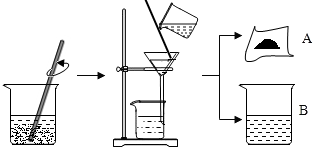
【猜想与假设】甲同学:只有CaCO3; 乙同学:CaCO3、Ca(OH)2
【实验与探究】甲、乙同学为了验证各自的猜想,分别进行了实验:
【反思与评价】小组同学讨论后认为,甲同学的实验不能证明他的猜想,理由是有气泡生成说明了含有碳酸钙,不能说明含有氢氧化钙;而乙同学的实验能证明他的猜想,因此小组同学确定了固体A的成分.
【提出问题2】溶液B中溶质的成分是什么?
【猜想与假设】丙同学:KOH、K2CO3;丁同学:KOH、Ca(OH)2
【表达与交流】结合对固体成分的探究,同学们经过讨论确定了丁同学猜想正确,理由是固体中含有氢氧化钙,说明了溶液为氢氧化钙的饱和溶液,溶液中含有氢氧化钙.为了得到纯净的氢氧化钾,需要向溶液B中滴加适量的一种溶液,发生反应的化学方程式为Ca(OH)2+K2C03=CaC03↓+2KOH,小组同学通过相应的实验操作最终制得了氢氧化钾.
【提出问题1】固体A中的成分是什么?

【猜想与假设】甲同学:只有CaCO3; 乙同学:CaCO3、Ca(OH)2
【实验与探究】甲、乙同学为了验证各自的猜想,分别进行了实验:
| 实验内容 | 实验现象 | 实验结论 |
| 甲同学:取少量固体于试管中,向其中加入稀盐酸. | 有气泡产生 | 猜想正确 反应方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑ |
| 乙同学:取少量固体于试管中,加水充分溶解、过滤,向滤液中滴加无色酚酞试液 | 溶液由无色变为红色 | 猜想正确 |
【提出问题2】溶液B中溶质的成分是什么?
【猜想与假设】丙同学:KOH、K2CO3;丁同学:KOH、Ca(OH)2
【表达与交流】结合对固体成分的探究,同学们经过讨论确定了丁同学猜想正确,理由是固体中含有氢氧化钙,说明了溶液为氢氧化钙的饱和溶液,溶液中含有氢氧化钙.为了得到纯净的氢氧化钾,需要向溶液B中滴加适量的一种溶液,发生反应的化学方程式为Ca(OH)2+K2C03=CaC03↓+2KOH,小组同学通过相应的实验操作最终制得了氢氧化钾.
12. 向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示.下列说法不正确的是( )
向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示.下列说法不正确的是( )
 向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示.下列说法不正确的是( )
向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示.下列说法不正确的是( )| A. | 取a点溶液,滴加稀盐酸,有白色沉淀 | |
| B. | 若取b~c段固体,滴加稀盐酸,有气泡产生 | |
| C. | c点溶液中的溶质为Zn(NO3)2 | |
| D. | d点时的固体有三种 |
13.下列化学用语表示离子的是( )
①P2O5 ②P ③CO32-④ ⑤$\stackrel{+2}{Mg}$.
⑤$\stackrel{+2}{Mg}$.
①P2O5 ②P ③CO32-④
 ⑤$\stackrel{+2}{Mg}$.
⑤$\stackrel{+2}{Mg}$.| A. | ①② | B. | ③④ | C. | ②④ | D. | ③⑤ |