题目内容
8.通过查阅资料得知:将熟石灰与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.为了制取氢氧化钾,兴趣小组的同学将少量熟石灰放入烧杯中,再向其中加入一定量碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B,操作步骤如图所示,请你与小组同学共同完成以下探究:【提出问题1】固体A中的成分是什么?
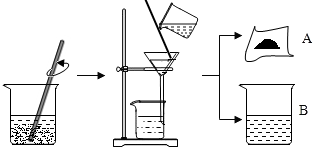
【猜想与假设】甲同学:只有CaCO3; 乙同学:CaCO3、Ca(OH)2
【实验与探究】甲、乙同学为了验证各自的猜想,分别进行了实验:
| 实验内容 | 实验现象 | 实验结论 |
| 甲同学:取少量固体于试管中,向其中加入稀盐酸. | 有气泡产生 | 猜想正确 反应方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑ |
| 乙同学:取少量固体于试管中,加水充分溶解、过滤,向滤液中滴加无色酚酞试液 | 溶液由无色变为红色 | 猜想正确 |
【提出问题2】溶液B中溶质的成分是什么?
【猜想与假设】丙同学:KOH、K2CO3;丁同学:KOH、Ca(OH)2
【表达与交流】结合对固体成分的探究,同学们经过讨论确定了丁同学猜想正确,理由是固体中含有氢氧化钙,说明了溶液为氢氧化钙的饱和溶液,溶液中含有氢氧化钙.为了得到纯净的氢氧化钾,需要向溶液B中滴加适量的一种溶液,发生反应的化学方程式为Ca(OH)2+K2C03=CaC03↓+2KOH,小组同学通过相应的实验操作最终制得了氢氧化钾.
分析 【实验与探究】甲、根据碳酸钙能与盐酸反应生成二氧化碳分析回答;
乙、根据氢氧化钙溶液显碱性分析回答;
【反思与评价】根据碳酸钙与盐酸反应生成了气体不能证明氢氧化钙是否存在分析;
【表达与交流】根据碳酸钾能与氢氧化钙分析回答.
解答 解:【实验与探究】由于碳酸钙能与盐酸反应生成了二氧化碳气体,所以,由甲同学取少量固体于试管中,向其中加入稀盐酸由气泡生成,证明了存在碳酸钙;由于氢氧化钙溶液显碱性,能使酚酞试液变红色,所以,甲、乙同学为了验证各自的猜想,分别进行了实验,填表如下:
| 实验内容 | 实验现象 | 实验结论 |
| 甲同学:取少量固体于试管中,向其中加入稀盐酸. | 有气泡产生 | 猜想正确 反应方程式为 CaCO3+2HCl=CaCl2+H2O+CO2↑ |
| 乙同学:取少量固体于试管中,加水充分溶解、过滤,向滤液中滴加 无色酚酞试液 | 溶液由无色变为红色 | 猜想正确 |
【表达与交流】由于碳酸钾能与氢氧化钙反应,由过滤的固体中含有氢氧化钙,所以,溶液中含有氢氧化钙,不含有碳酸钾,所以丁同学猜想正确.为了得到纯净的氢氧化钾,需要向溶液B中滴加适量的碳酸钾溶液,发生反应的化学方程式为 Ca(OH)2+K2C03=CaC03↓+2KOH,小组同学通过相应的实验操作最终制得了氢氧化钾.
故答为:【实验与探究】见上表;
【反思与评价】有气泡生成说明了含有碳酸钙,不能说明含有氢氧化钙;
【表达与交流】丁,Ca(OH)2+K2C03=CaC03↓+2KOH.
点评 本考点既考查了实验步骤的设计,又考查了化学方程式的书写,还对实验进行了评价,综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
17.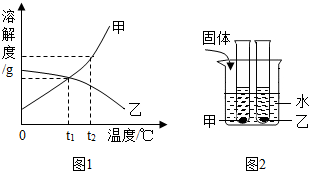 如图所示,图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管 (不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )
如图所示,图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管 (不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )
 如图所示,图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管 (不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )
如图所示,图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管 (不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )| A. | t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为:甲>乙 | |
| B. | 将甲、乙两种物质的饱和溶液都从t2℃降到t1℃时,两种溶液中溶质质量分数相等 | |
| C. | 向烧杯的水中加氧化钙固体后,只有乙溶液中溶质的质量分数变小 | |
| D. | 甲物质中含有少量的乙物质时,可采取冷却热饱和溶液的方法获得甲物质 |
15.镁是一种用途广泛的金属材料,目前使用的镁主要是从海水中提取的,主要流程如图所示.
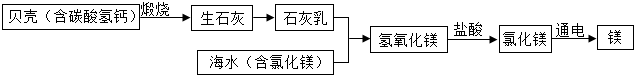
上述转化过程中未涉及到的基本反应类型是( )

上述转化过程中未涉及到的基本反应类型是( )
| A. | 分解反应 | B. | 化合反应 | C. | 置换反应 | D. | 复分解反应 |
20.下列有关硬水的说法不正确的是( )
| A. | 明矾常用于净水,可以使硬水软化 | |
| B. | 硬水和软水可用肥皂水鉴别 | |
| C. | 硬水中的Ca(HCO3)2、Mg(HCO3)2可用加热煮沸法除去 | |
| D. | 蒸馏法可比较彻底的除去硬水中的Ca2+、Mg2+,蒸馏装置冷凝管中的冷凝水应下进上出 |
17.下列生活用品的主要材质属于有机合成材料的是( )
| A. |  玻璃杯 | B. |  羊毛围巾 | C. |  塑料水盆 | D. |  木质桌椅 |
18.下列关于物质用途的叙述,易造成重大伤亡事故的是( )
| A. | 活性炭可做冰箱除臭剂 | B. | 庆典活动可使用大量氢气球 | ||
| C. | 熟石灰可用来粉墙 | D. | 钛合金可做轮船外壳 |

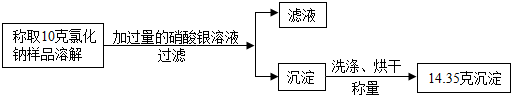
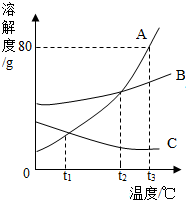 如图是A、B、C三种物质的溶解度随温度变化的曲线图.根据如图回答:
如图是A、B、C三种物质的溶解度随温度变化的曲线图.根据如图回答: