题目内容
5. 实验小组在研究酸和碱的化学性质时,对稀硫酸与NaOH溶液的反应展开探究,请完成他们的探究记录.
实验小组在研究酸和碱的化学性质时,对稀硫酸与NaOH溶液的反应展开探究,请完成他们的探究记录.【提出问题】稀硫酸与NaOH溶液混合后是否发生了化学反应?
【查阅资料】①稀硫酸与NaOH溶液混合后,虽然没有明显现象,但确实发生了化学反应,如图是反应的微观示意图,从该图可以看出,稀硫酸与NaOH溶液反应的本质是氢离子与氢氧根离子结合成水分子;
②NaOH溶液能与硫酸铜溶液反应,化学反应方程式为:2NaOH+CuSO4═Cu(OH)2↓+Na2SO4;
【实验器材】NaOH溶液、稀硫酸、酚酞试液、pH试纸、烧杯、玻璃棒、胶头滴管、试管、镊子、玻璃片等.
【实验探究】实验小组设计了三个方案进行实验.
| 实验操作 | 实验现象或数据 | 实验结论 | |
| 方案1 | 取少量NaOH溶液于试管中,测定其pH,将一定量的稀硫酸倾倒入该溶液中,混合均匀后测定其pH | NaOH溶液的pH>7,混合均匀后溶液的pH<7 | 稀硫酸与NaOH溶液混合后发生了化学反应, 且方案1中稀硫酸过量 |
| 方案2 | 取少量NaOH溶液倒入烧杯中,滴入几滴酚酞试液,再用滴管逐滴滴入稀硫酸,并用玻璃棒不断搅拌 | 溶液由红色变为无色 | |
| 方案3 | 取少量稀硫酸于试管中,倒入少量硫酸铜溶液,再用滴管逐滴滴入NaOH溶液,边滴边振荡 | 开始无明显现象,滴入一定量NaOH溶液后有蓝色沉淀产生 |
(2)由方案2和方案3可知,对于许多没有明显现象的化学反应,可通过滴加其他试剂,使其产生明显现象的方法以证明反应确实发生了.
分析 [查阅资料]根据反应前后离子的不同来进行解答;
[实验探究]酚酞遇酸性和中性溶液不变色,可以据此来完成方案2的现象;氢氧化钠和稀硫酸恰好完全反应时,加入硫酸铜不会产生沉淀,但是可以和氢氧化钠反应生成沉淀,可以据此解答;
[反思交流](1)根据测定pH的方法来解答;
(2)对于许多没有明显现象的化学反应通常借助于其它试剂来帮助判断,可以据此解答.
解答 解:[查阅资料]比较反应前后离子可以知道,该反应的实质是氢氧根离子和氢离子反应生成了水分子;
[实验探究]酚酞遇酸性和中性溶液不变色,所以我们能够观察到方案2中溶液由红色变为无色;氢氧化钠和稀硫酸恰好完全反应时,加入硫酸铜不会产生沉淀,但是可以和氢氧化钠反应生成沉淀,所以可以观察到开始时没有蓝色沉淀产生,当加入氢氧化钠溶液之后产生了蓝色沉淀;
[反思交流](1)测定pH值时要注意保证玻璃棒的干燥和洁净,所以每使用玻璃棒蘸取溶液前,必须进行洗净并擦干的预处理;
(2)对于许多没有明显现象的化学反应通常借助于其它试剂来帮助判断.
故答案为:[查阅资料]氢离子与氢氧根离子结合成水分子;
[实验探究]
| 实验操作 | 实验现象或数据 | 实验结论 | |
| 方案1 | 取少量NaOH溶液于试管中,测定其pH,将一定量的稀硫酸倾倒入该溶液中,混合均匀后测定其pH | NaOH溶液的pH>7,混合均匀后溶液的pH<7 | 稀硫酸与NaOH溶液混合后发生了化学反应, 且方案1中 稀硫酸过量 |
| 方案2 | 取少量NaOH溶液倒入烧杯中,滴入几滴酚酞试液,再用滴管逐滴滴入稀硫酸,并用玻璃棒不断搅拌 | 溶液由红色变为无色 | |
| 方案3 | 取少量稀硫酸于试管中,倒入少量硫酸铜溶液,再用滴管逐滴滴入NaOH溶液,边滴边振荡 | 开始无明显现象,滴入一定量NaOH溶液后有蓝色沉淀产生 |
点评 本题考查了酸碱中和反应,完成此题,可以依据已有的知识进行,所以要求同学们在平时的学习中加强基础知识的储备.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
17.某同学从C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2中获得以下信息:①该反应的反应物是碳和氧气②反应发生条件是点燃③反应前后元素种类和原子个数不变④反应前后分子总数保持不变⑤参加反应的碳和氧气的质量比为3:8,其中正确的信息是( )
| A. | ①②③④ | B. | ①②③⑤ | C. | ①②④⑤ | D. | ②③④⑤ |
20. 黄金是一种贵重金属,结合如图,下列有关金元素说法正确的是( )
黄金是一种贵重金属,结合如图,下列有关金元素说法正确的是( )
 黄金是一种贵重金属,结合如图,下列有关金元素说法正确的是( )
黄金是一种贵重金属,结合如图,下列有关金元素说法正确的是( )| A. | 核电荷数为276 | B. | 原子序数为118 | ||
| C. | 中子数为79 | D. | 相对原子质量为197.0 |
14.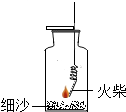 做完“铁在氧气里燃烧”的实验后,某兴趣小组有一些疑惑不解的问题,于是进行了以下探究:
做完“铁在氧气里燃烧”的实验后,某兴趣小组有一些疑惑不解的问题,于是进行了以下探究:
【问题一】细铁丝在氧气中燃烧为什么会火星四射?
【查阅资料1】铁制品一般含有少量碳,含碳细铁丝燃烧时,炭粒生成的二氧化碳在熔融态物质中形成气泡,熔融态物质因气泡炸裂引起火星四射现象.
【设计实验】为了探究火星四射现象的原因,该小组同学设计的实验方案是:
取长短粗细相同的含碳细铁丝和不含碳的细铁丝,分别在足量的氧气中燃烧,观察现象.
【实验探究1】小明按如图所示装置做细铁丝在氧气中燃烧的实验.
但不见铁丝燃烧,反复实验均未成功.写出导致该同学实验失败的可能原因(两个 ):铁丝表面有锈迹,影响了反应的进行、点燃火柴后立即将它伸入瓶内,火柴燃烧消耗了氧气,不利于铁丝的燃烧
经过改进,该同学完成了该实验,写出反应的文字表达式铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
【问题2】铁燃烧时溅落下来的黑色物质中还有没有铁?
【查阅资料2】自然界中铁的氧化物主要有三氧化二铁和四氧化三铁两种(三氧化二铁为暗红色,氧化亚铁极易被氧化为三氧化二铁).
【实验探究2】将冷却后的黑色物质碾碎,装入试管,加入足量稀盐酸,产生气泡,说明溅落下来的黑色物质中还有铁.
【问题3】铁燃烧的产物为什么不是三氧化二铁呢?
【查阅资料3】①三氧化二铁和四氧化三铁的分解温度见下表;②三氧化二铁高温分解成四氧化三铁
【理论讨论】根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温在1535℃~1538℃之间,此温度范围三氧化二铁已分解.
【拓展延伸】①三氧化二铁高温分解成四氧化三铁和一种气体,写出该反应的文字表达式三氧化二铁$\stackrel{高温}{→}$四氧化三铁+氧气;
②有些超市的食品包装盒放有黑色的氧化亚铁粉末,若粉末的颜色变成暗红色,就说明包装盒漏气,售货员就能及时发现并处理.
 做完“铁在氧气里燃烧”的实验后,某兴趣小组有一些疑惑不解的问题,于是进行了以下探究:
做完“铁在氧气里燃烧”的实验后,某兴趣小组有一些疑惑不解的问题,于是进行了以下探究:【问题一】细铁丝在氧气中燃烧为什么会火星四射?
【查阅资料1】铁制品一般含有少量碳,含碳细铁丝燃烧时,炭粒生成的二氧化碳在熔融态物质中形成气泡,熔融态物质因气泡炸裂引起火星四射现象.
【设计实验】为了探究火星四射现象的原因,该小组同学设计的实验方案是:
取长短粗细相同的含碳细铁丝和不含碳的细铁丝,分别在足量的氧气中燃烧,观察现象.
【实验探究1】小明按如图所示装置做细铁丝在氧气中燃烧的实验.
但不见铁丝燃烧,反复实验均未成功.写出导致该同学实验失败的可能原因(两个 ):铁丝表面有锈迹,影响了反应的进行、点燃火柴后立即将它伸入瓶内,火柴燃烧消耗了氧气,不利于铁丝的燃烧
经过改进,该同学完成了该实验,写出反应的文字表达式铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
【问题2】铁燃烧时溅落下来的黑色物质中还有没有铁?
【查阅资料2】自然界中铁的氧化物主要有三氧化二铁和四氧化三铁两种(三氧化二铁为暗红色,氧化亚铁极易被氧化为三氧化二铁).
【实验探究2】将冷却后的黑色物质碾碎,装入试管,加入足量稀盐酸,产生气泡,说明溅落下来的黑色物质中还有铁.
【问题3】铁燃烧的产物为什么不是三氧化二铁呢?
【查阅资料3】①三氧化二铁和四氧化三铁的分解温度见下表;②三氧化二铁高温分解成四氧化三铁
| 四氧化三铁 | 三氧化二铁 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | --- |
| 溶点/℃ | --- | --- | 1535 |
【拓展延伸】①三氧化二铁高温分解成四氧化三铁和一种气体,写出该反应的文字表达式三氧化二铁$\stackrel{高温}{→}$四氧化三铁+氧气;
②有些超市的食品包装盒放有黑色的氧化亚铁粉末,若粉末的颜色变成暗红色,就说明包装盒漏气,售货员就能及时发现并处理.

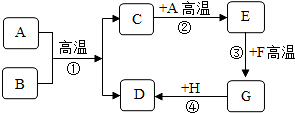 图中A-H都是初中化学中常见的物质,已知A、B都是黑色固体,D、F为红色固体,它们之间的转化关系如图所示,请推断出各物质后解答下列问题:
图中A-H都是初中化学中常见的物质,已知A、B都是黑色固体,D、F为红色固体,它们之间的转化关系如图所示,请推断出各物质后解答下列问题: