题目内容
14. 一氧化碳气体在生产生活中有着广泛的应用.请回答下列问题:
一氧化碳气体在生产生活中有着广泛的应用.请回答下列问题:(1)物质的性质决定其用途.因为一氧化碳具有可燃性,所以可用作燃料.
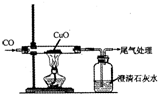
(2)如图是一氧化碳还原氧化铜的实验.请指出实验中能证明发生了化学变化的证据黑色粉末变成红色或澄清石灰水变浑浊(写一条).
分析 (1)从物质的性质决定其用途,一氧化碳的性质去分析;
(2)从一氧化碳还原氧化铜的实验时,所观察到的现象是:黑色粉末变成红色,说明反应生成铜;澄清石灰水变浑浊,说明生成二氧化碳气体去分析.
解答 解:(1)由于一氧化碳具有可燃性,所以可用做燃料;故答案为:可燃;
(2)一氧化碳还原氧化铜的实验时,所观察到的现象是:黑色粉末变成红色,说明反应生成铜;澄清石灰水变浑浊,说明生成二氧化碳气体.化学变化的特征是产生了新物质,故上述两个现象都说明产生了新的物质;故答案为:黑色粉末变成红色或澄清石灰水变浑浊.
点评 本题综合考查了一氧化碳的化学性质,是基础知识,难度不大.

练习册系列答案
相关题目
2.锂元素(元素符号为Li)及其所形成的化合物,在通讯和航空航天领域中具有极其重要的用途.它的化合物氢氧化锂(LiOH)是一种易溶于水的白色固体,有辣味,具有强碱性和腐蚀性.
(1)氢氧化锂属于碱(填“酸”、“碱”、“盐”或金属氧化物).
(2)写出氢氧化锂与硫酸(H2SO4)反应的化学方程式2LiOH+H2SO4═Li2SO4+2H2O;
(3)上表是部分物质的溶解性表,运用此溶解性表并结合你对复分解反应发生条件的理解,从表中选出一种盐,该盐能和LiOH发生复分解反应,请你写出该反应的化学方程式:2LiOH+CuSO4═Li2SO4+Cu(OH)2↓.
(1)氢氧化锂属于碱(填“酸”、“碱”、“盐”或金属氧化物).
(2)写出氢氧化锂与硫酸(H2SO4)反应的化学方程式2LiOH+H2SO4═Li2SO4+2H2O;
| OH- | CO32- | SO42- | NO3- | |
| Ba2+ | 溶 | 不 | 不 | 溶 |
| Cu2+ | 不 | 不 | 溶 | 溶 |
| Li+ | 溶 | 微溶 | 溶 | 溶 |
9.下列各组物质中,俗名、化学名称和化学式表示的不是同一种物质的是( )
| A. | 熟石灰、氢氧化钙、Ca(OH)2 | B. | 烧碱、碳酸钠、Na2CO3 | ||
| C. | 盐酸、氯化氢水溶液、HCl | D. | 食盐、氯化钠、NaCl |
19.某兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验.请你与他们一起完成以下探究活动:
【对固体猜想】
猜想I:全部是NaOH
猜想Ⅱ:全部是Na2CO3
猜想Ⅲ:部分是NaOH,部分是Na2CO3.
【实验和推断】
(1)若现象A为有气泡产生,则加入的X溶液是稀盐酸,说明氢氧化钠已经变质.
(2)若X是Ca(OH)2溶液,现象A有白色沉淀,现象B为无色酚酞试液变红色,该实验不能(填“能”或“不能”)说明样品中有NaOH,原因加入Ca(OH)2溶液会带入OH-离子或与Na2CO3反应可以生成NaOH,对实验产生干扰.
(3)若猜想Ⅲ成立,则X是CaCl2溶液.
【反思应用】
(4)保存NaOH溶液的方法是密封保存.
【对固体猜想】
猜想I:全部是NaOH
猜想Ⅱ:全部是Na2CO3
猜想Ⅲ:部分是NaOH,部分是Na2CO3.
【实验和推断】
| 实验步骤 | 实验现象 |
| ①取少量白色固体于试管中,加水至全部溶解. | 无色溶液 |
| ②向溶液中滴加适量物质X的溶液. | 现象A |
| ③再向试管中滴加几滴酚酞试液. | 现象B |
(2)若X是Ca(OH)2溶液,现象A有白色沉淀,现象B为无色酚酞试液变红色,该实验不能(填“能”或“不能”)说明样品中有NaOH,原因加入Ca(OH)2溶液会带入OH-离子或与Na2CO3反应可以生成NaOH,对实验产生干扰.
(3)若猜想Ⅲ成立,则X是CaCl2溶液.
【反思应用】
(4)保存NaOH溶液的方法是密封保存.
6.下列转化能由一步反应实现的是( )
| A. | FeO→Fe(OH)2 | B. | CuO→Cu(OH)2 | C. | CaCO3→Ca(OH)2 | D. | BaCl2→Ba(NO3)2 |
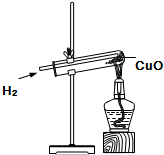 如图所示是氢气和氧化铜反应的实验装置图.请分析回答:
如图所示是氢气和氧化铜反应的实验装置图.请分析回答: