题目内容
7.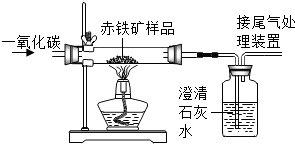 高炉炼铁的主要原料是赤铁矿石(主要成分为Fe2O3)、焦炭、空气等,主要反应流程如图所示:
高炉炼铁的主要原料是赤铁矿石(主要成分为Fe2O3)、焦炭、空气等,主要反应流程如图所示:[焦炭]$\stackrel{反应(a)}{→}$[二氧化碳]$\stackrel{反应(b)}{→}$[一氧化碳]$\stackrel{反应(c)}{→}$[铁]
写出上述反应的化学方程式:
(1)反应(a)C+O2$\frac{\underline{\;高温\;}}{\;}$CO2
(2)反应(b)CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO
(3)反应(c)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(4)用如图所示装置模拟反应(c),已知反应前赤铁矿的质量为10g,反应一段时间后固体质量变为8.4g,求参加反应的CO的质量为2.8g.
(5)尾气应怎样处理:点燃.
分析 高炉炼铁的高炉中发生一系列化学变化,首先焦炭与空气中的氧气生成二氧化碳,然后生成的二氧化碳继续与焦炭反应生成气体还原剂一氧化碳,接下来一氧化碳还原氧化铁生成铁和二氧化碳,从而冶炼得到生铁.
已知反应前赤铁矿的质量为10g,反应一段时间后,剩余固体的质量为8.4g,可结合反应的化学方程式利用差量法进行分析解答;
根据根据一氧化碳有毒和能燃烧的性质考虑尾气处理;
解答 解:(1)焦炭为单质碳,在高温条件下与空气中氧气反应生成二氧化碳;故答案为:C+O2$\frac{\underline{\;高温\;}}{\;}$CO2;
(2)二氧化碳在高温条件下,与焦炭继续发生化合反应生成具有还原性的气体一氧化碳;故答案为:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
(3)一氧化碳在高温条件下,与赤铁矿石中的氧化铁发生氧化还原反应,生成铁和二氧化碳;故答案为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(4)解:参加反应的CO的质量为x,
固体减少的质量是10g-8.4g=1.6g
3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 差量
84 160 112 48
x 10g-8.4g=1.6g
则$\frac{84}{x}=\frac{48}{1.6g}$,解得x=2.8g
答:参加反应的CO的质量为2.8g.
(4)根据根据一氧化碳有毒和能燃烧的性质考虑尾气处理;所以点燃尾气生成二氧化碳,排到空气中;
故答案为:
(1)C+O2$\frac{\underline{\;高温\;}}{\;}$CO2;(2)CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;(3)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(4)2.8.(5)点燃.
点评 高炉炼铁是利用焦炭先后与氧气、二氧化碳反应形成气体还原剂一氧化碳,然后利用一氧化碳还原氧化铁得到铁和二氧化碳.

| A. | 劈柴引火-使温度达到煤的着火点 | B. | 扇子扇风-为燃料提供足够的氧气 | ||
| C. | 蓝色火焰-一氧化碳在燃烧 | D. | 放一壶水-防止煤气中毒 |
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬( CrSO4)溶液.
【假设】三种金属在金属活动性顺序中的相对位置关系:
①Cr>Al>Cu ②Al>Cr>Cu ③Al>Cu>Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮,进行以下实验探究:
| 实验一 | 实验二 | 实验三 | |
| 实验 方案 | 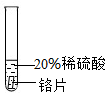 | 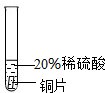 | 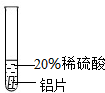 |
| 实验 现象 | 铬片表面产生气泡缓慢,溶液 变蓝色. | 无现象 | 铝片表面产生气泡较快. |
| 结论[ | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | 铝能与稀硫酸发生反应,反应速率较快 |
| 原假设中正确的是②.(填序号) | |||
(2)实验一所发生反应的化学方程式是Cr+H2SO4=CrSO4+H2↑.
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是Al、Cr都能与硫酸铜溶液发生反应.
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是Al、CrSO4溶液、Cu(合理答案均即可).
| A. | 活海鲜中通O2 | B. | 制成干货 | C. | 用甲醛浸泡保鲜 | D. | 冷冻 |
| A. | 用稀盐酸除去铁锈:Fe2O3+4HCl═2FeCl2+2H2O | |
| B. | 白磷自燃:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | |
| C. | 电解水:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2↑ | |
| D. | 实验室制备H2:Zn+H2SO4═ZnSO4+H2↑ |
| A. | 将大块煤粉碎后再燃烧,其目的是延迟煤燃烧的时间 | |
| B. | 火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点 | |
| C. | 室内失火不能打开门窗,是因为空气流动加快使燃烧更剧烈 | |
| D. | 蜡烛用扇子一扇即灭,是因为带走了蜡烛周围的空气 |
| A. | 蔗糖溶解 | B. | 干冰升华 | C. | 食物腐败变质 | D. | 木材做成桌椅 |