��Ŀ����
2��þ��һ����;�ܹ�Ľ������Ӻ�ˮ����ȡþ����Ҫ������ͼ��ʾ���������һ��̽����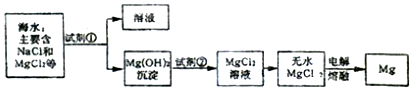
��1���Լ��ٵ�����Ϊ�������ƣ�����õ�Mg��OH��2��������Һ�Ļ���ʵ�����Ϊ���ˣ��������������
��2��д���Լ��������ʵĻ�ѧʽHCl������Mg��OH��2������ѧ��Ӧ�Ļ�ѧ����ʽΪMg��OH��2+2HCl�TMgCl2+2H2O��
��3���Ȼ�þ�����Σ������������ᡱ��������Ρ���������״̬����ˮ�Ȼ�þͨ��Ļ�ѧ��Ӧ���ڷֽⷴӦ���������Ӧ���ͣ���
���� �Ȼ�þ���������Ʒ�Ӧ����������þ�������Ȼ��ƣ�������þ��ϡ���ᷴӦ�����Ȼ�þ��ˮ��
����״̬����ˮ�Ȼ�þͨ��ֽ�����þ��������
��� �⣺��1���Լ��ٵ�����Ϊ�������ƣ�
����õ�Mg��OH��2��������Һ�Ļ���ʵ������ǹ��ˣ�
����������ƣ����ˣ�
��2���Լ�����ϡ���ᣬϡ���������ʵĻ�ѧʽ��HCl��
ϡ������Mg��OH��2������ѧ��Ӧ�����Ȼ�þ��ˮ����Ӧ�Ļ�ѧ����ʽΪ��Mg��OH��2+2HCl�TMgCl2+2H2O��
���HCl��Mg��OH��2+2HCl�TMgCl2+2H2O��
��3���Ȼ�þ�����Σ�
����״̬����ˮ�Ȼ�þͨ��ֽ�����þ�����������ڷֽⷴӦ��
����Σ��ֽ⣮
���� ������Ҫ�������ʵ����ʣ����ʱҪ���ݸ������ʵ����ʣ���ϸ������������з������жϣ��Ӷ��ó���ȷ�Ľ��ۣ�

��ϰ��ϵ�д�
�����Ŀ
17���ҹ���ѧ�Һ��ġ������Ƽ�����ռ��Ч�ʸߣ�����Ҫ��Ӧ���£�
��NH3+H2O+CO2�TNH4HCO3
��NaCl�����ͣ�+NH4HCO3�TNH4C1+NaHCO3��
��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2��
����˵����ȷ���ǣ�������
��NH3+H2O+CO2�TNH4HCO3
��NaCl�����ͣ�+NH4HCO3�TNH4C1+NaHCO3��
��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2��
����˵����ȷ���ǣ�������
| A�� | �ڷ�Ӧ�Ǹ��ֽⷴӦ | |
| B�� | �۷�Ӧ������̼Ԫ�صĻ��ϼ۷����˸ı� | |
| C�� | �۷�Ӧ���H2O��CO2���Ա�ѭ��ʹ�� | |
| D�� | ��Ӧ������ֻ�õ�һ�ֲ���Na2CO3 |
7��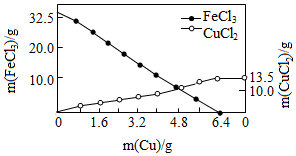 FeCl3��Һ������ʴ��ӡˢ��·����Ӧԭ��ΪaFeCl3+bCu�TcCuCl2+dX��������32.5g��FeCl3��Һ����������һ������Cu�ۣ���Ӧ������FeCl3��CuCl2��������Cu�������仯��ͼ������˵������ȷ���ǣ�������
FeCl3��Һ������ʴ��ӡˢ��·����Ӧԭ��ΪaFeCl3+bCu�TcCuCl2+dX��������32.5g��FeCl3��Һ����������һ������Cu�ۣ���Ӧ������FeCl3��CuCl2��������Cu�������仯��ͼ������˵������ȷ���ǣ�������
 FeCl3��Һ������ʴ��ӡˢ��·����Ӧԭ��ΪaFeCl3+bCu�TcCuCl2+dX��������32.5g��FeCl3��Һ����������һ������Cu�ۣ���Ӧ������FeCl3��CuCl2��������Cu�������仯��ͼ������˵������ȷ���ǣ�������
FeCl3��Һ������ʴ��ӡˢ��·����Ӧԭ��ΪaFeCl3+bCu�TcCuCl2+dX��������32.5g��FeCl3��Һ����������һ������Cu�ۣ���Ӧ������FeCl3��CuCl2��������Cu�������仯��ͼ������˵������ȷ���ǣ�������| A�� | XΪFeCl2 | B�� | ��ѧ������c=1 | ||
| C�� | ����ʽ��a��b�ı�Ϊ1��2 | D�� | ��ȫ��Ӧ������X������Ϊ25.4g |
14������ѧ��ͨ���ⶨ�����ź��е�̼-14�������ƶ����������̼-14ԭ�ӵĺ˵����Ϊ6�����ԭ������Ϊ14�����й���̼-14ԭ�ӵ�˵���У�������ǣ�������
| A�� | ������Ϊ14 | B�� | ������Ϊ6 | ||
| C�� | ������Ϊ6 | D�� | ��������������ֵ֮��Ϊ14 |
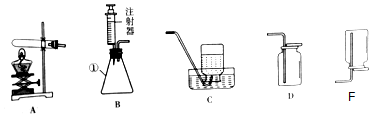
11����ͼ��ʾ��ʵ�������ȷ���ǣ�������
| A�� |  ϡ��Ũ���� | B�� |  �����Ȼ�����Һ | C�� |  �ⶨ��Һ��pH | D�� |  �����ᾧ |