题目内容
14.某同学利用“多米诺骨牌”效应,设计了如下气体制取与性质验证的组合实验.打开A中分液漏斗的活塞,很快看到E中导管口有气泡冒出,且溶液由紫色变红色.看图回答问题:
(1)A中反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)C、D中看到的现象分别是C中液面下降、稀盐酸进入D,产生大量气泡.
(3)用化学方程式表示E中颜色变化的原因CO2+H2O=H2CO3用F装置收集气体的依据是二氧化碳的密度比空气大.
分析 (1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(2)氧气不易溶于水,进入C装置会使C装置中气体压强增大,稀盐酸进入D,稀盐酸与石灰石反应生成二氧化碳;
(3)显酸性的溶液能使石蕊试液变红色;二氧化碳密度比空气大;
解答 解:(1)过氧化氢在常温下用二氧化锰做催化剂反应生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)氧气不易溶于水进入C装置后会使C装置中气体压强增大,稀盐酸会被压入D装置,稀盐酸与石灰石反应生成氯化钙水和二氧化碳气体;故填:C中液面下降;稀盐酸进入D,产生大量气泡;
(3)E中紫色石蕊试液变红说明生成了酸,二氧化碳与水反应生成碳酸;二氧化碳的密度比空气大可以用向上排空气法收集;故填:CO2+H2O=H2CO3;二氧化碳的密度比空气大;
点评 此题考查有关氧气的制取和二氧化碳的制取和性质,掌握相应的知识点是解答的关键,在初中掌握三大气体的制备原理、制备装置、收集方法、检验方法、验满方法等知识点非常重要,平时学习中要给予关注.

练习册系列答案
相关题目
4.形态各异的物质可按一定规律分类.现有以下八种物质,请选用各物质名称前的字母序号填在相应位置.
A.盐酸 B.氯化钾C.氧化铜 D.淀粉E.五氧化二磷 F.氮气G.氢氧化钙 H.甲烷
A.盐酸 B.氯化钾C.氧化铜 D.淀粉E.五氧化二磷 F.氮气G.氢氧化钙 H.甲烷
| 题号 | 物质分类标准 | 字母序号 | 题号 | 物质分类标准 | 字母序号 |
| (1) | 金属氧化物 | (5) | 非金属单质 | ||
| (2) | 非金属氧化物 | (6) | 挥发性酸 | ||
| (3) | 易溶性盐 | (7) | 最简单 的有机物 | ||
| (4) | 微溶性碱 | (8) | 糖类 |
9.下列有关碳循环的说法错误的是( )
| A. | 绿色植物光合作用吸收CO2释放O2 | |
| B. | 提倡“低碳生活”,大力推广风能、太阳能等新能源 | |
| C. | 用石灰水吸收空气中过量的CO2,以解决温室效应 | |
| D. | 动、植物呼吸作用吸收O2释放CO2 |
19.下列物质的化学式书写正确的是( )
| A. | 氧化铝AlO | B. | 氦气He2 | C. | 氯化亚铁FeCl3 | D. | 氢氧化钠 NaOH |
3.(1)如图I是利用排水法收集的某无色气体.请据此回答该气体应具有的物理性质(色态味除外)密度大于空气.
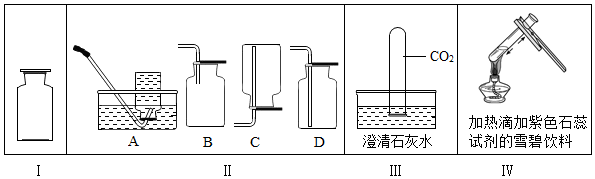
(2)请你用学过的知识进行探究,确定图I无色气体的成分.
(3)如图Ⅱ装置所示,CO2气体的收集方法正确的是D.
(4)如图Ⅲ所示,将收集到的一个充满纯净的二氧化碳气体的试管倒置于澄清的石灰水中,同时轻轻震荡,可观察到的现象是:①溶液变浑浊②试管内液面上升.
(5)如图Ⅳ所示,该实验的现象是溶液由红色变为紫色,出现此现象的原因碳酸不稳定,加热会分解,酸性消失.

(2)请你用学过的知识进行探究,确定图I无色气体的成分.
| 假设(猜想) | 验证操作 | 可能看到的现象 | 结论 |
| 氧气 | 将带火星的木条伸进集气瓶内 | 木条复燃 | 为猜想气体 |
(4)如图Ⅲ所示,将收集到的一个充满纯净的二氧化碳气体的试管倒置于澄清的石灰水中,同时轻轻震荡,可观察到的现象是:①溶液变浑浊②试管内液面上升.
(5)如图Ⅳ所示,该实验的现象是溶液由红色变为紫色,出现此现象的原因碳酸不稳定,加热会分解,酸性消失.
