题目内容
8.实验室里有氯酸钾、二氧化锰、稀硫酸、石灰石和稀盐酸等五种药品,以及下列仪器: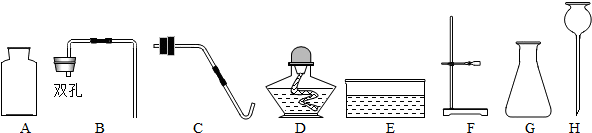
(1)制取二氧化碳所用到的仪器除A、B外,还需要用到G和H,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)制取氧气还需补充的仪器是试管(填仪器名称),写出用上述药品制氧气的化学方程式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
分析 (1)实验室制取二氧化碳的反应原理是:利用石灰石和稀盐酸在常温下反应来制取二氧化碳;
(2)实验室制取氧气的反应原理是:采用分解过氧化氢溶液、加热氯酸钾或加热高锰酸钾.
解答 解:(1)实验室用石灰石和稀盐酸反应制取二氧化碳,选用“固+液 常温”型装置,应选择的仪器集气瓶、双孔橡皮塞、锥形瓶和长颈漏斗,药品是石灰石和稀盐酸,反应的化学方程式是 CaCO3+2HCl=CaCl2+H2O+CO2↑.
故填:G,H,CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)若再利用上述仪器和药品制取氧气,应补充盛放药品的能用来加热的仪器--试管,反应还需要集气瓶、单孔橡皮塞和导管、酒精度、铁架台等,二氧化锰做反应的催化剂,反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
故填:试管;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
故答案为:
(1)G,H,CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)试管,2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
点评 利用所给的仪器和药品来制取气体时,首先考虑制取某种气体用到什么药品,所给药品中是否有,如果有了再考虑用到什么仪器,所给的仪器中是否都有,按照这样的思路考虑.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
18.下列曲线图与实验事实一致的是( )


| A. | 图①是向一定量的制取CO2后残留的酸性废水中加入过量Na2CO3溶液 | |
| B. | 图②是在一定温度下,向一定量饱和NaCl溶液中不断加入蔗糖 | |
| C. | 图③是用酒精灯加热一定质量的KMnO4固体 | |
| D. | 图④是向一定量的盐酸中滴加氢氧化钠溶液 |
19.区分下列各组物质的两种方法均正确的是( )
| 选项 | 需区分物质 | 方法一 | 方法二 |
| A | 硝酸铵和硫酸钾 | 加氢氧化钙研磨 | 加适量水触摸烧杯 |
| B | 硬水和软水 | 仔细观察是否浑浊 | 分别加适量肥皂水振荡 |
| C | 羊毛制品和纯棉制品 | 观察颜色 | 点燃闻气味 |
| D | 纯碱和食盐 | 配溶液,测pH | 分别加水,看能否溶解 |
| A. | A | B. | B | C. | C | D. | D |
16.下列叙述不正确的是( )
| A. | 化学反应前后原子种类不变 | |
| B. | 金刚石、石墨、C60都是碳元素的单质 | |
| C. | NO2的一个分子里含有两个氧原子 | |
| D. | 化学变化中原子的核外电子数都保持不变 |
3.在①金刚石②石墨③二氧化碳④二氧化硫⑤天然气⑥氢气等物质中,选择填空:
| 固体俗称“干冰”的物质 | 硬度最大的物质 | 有刺激性气味的气体 | 最理想的清洁燃料 | 铅笔芯的主要成分 | 属于化石燃料的物质 |
| ③ | ① | ④ | ⑥ | ② | ⑤ |
13.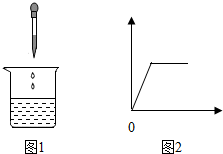 向盛有某溶液的烧杯中逐滴加入X溶液至过量(图1),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图2的是( )
向盛有某溶液的烧杯中逐滴加入X溶液至过量(图1),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图2的是( )
 向盛有某溶液的烧杯中逐滴加入X溶液至过量(图1),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图2的是( )
向盛有某溶液的烧杯中逐滴加入X溶液至过量(图1),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图2的是( ) | 烧杯中的物质 | X溶液 | |
| A | 稀硫酸和稀盐酸 | 氯化钡溶液 |
| B | 稀硫酸和硫酸铜溶液 | 氢氧化钠溶液 |
| C | 澄清石灰水 | 碳酸钠溶液 |
| D | 碳酸氢钠溶液 | 稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
20.同学们在实验室用混合两种固体药品的办法自制“钾、氮复合肥料”,使用到的药品有KCl,K2SO4,NH4HCO3,NH4Cl.同学们制得了成分不同的“钾,氮复合肥料”,从中抽取一份作为样品探究其成分,请回答有关问题:
限选试剂:稀H2SO4,BaCl2溶液,AgNO3溶液,蒸馏水
(1)提出合理假设.所抽样品的成分有4种可能:
假设1:KCl和NH4HCO3;假设2:KCl和NH4Cl;
假设3:K2SO4和NH4HCO3;假设4:K2SO4和NH4Cl.
(2)形成设计思路.
①甲同学提出先用AgNO3溶液确定是否含有KCl,你是否同意并说出理由:不同意,因为氯化铵和硝酸银反应也能够生成白色沉淀氯化银.
②乙同学提出先确定是否含有NH4HCO3,他认为不用其它试剂就可确定的理由是碳酸氢铵能和稀盐酸反应生成氯化铵、水和二氧化碳或能和稀硫酸反应生成硫酸铵、水和二氧化碳.
(3)完成实验方案.请填写实验操作,与表中结论相符的预期现象.
限选试剂:稀H2SO4,BaCl2溶液,AgNO3溶液,蒸馏水
(1)提出合理假设.所抽样品的成分有4种可能:
假设1:KCl和NH4HCO3;假设2:KCl和NH4Cl;
假设3:K2SO4和NH4HCO3;假设4:K2SO4和NH4Cl.
(2)形成设计思路.
①甲同学提出先用AgNO3溶液确定是否含有KCl,你是否同意并说出理由:不同意,因为氯化铵和硝酸银反应也能够生成白色沉淀氯化银.
②乙同学提出先确定是否含有NH4HCO3,他认为不用其它试剂就可确定的理由是碳酸氢铵能和稀盐酸反应生成氯化铵、水和二氧化碳或能和稀硫酸反应生成硫酸铵、水和二氧化碳.
(3)完成实验方案.请填写实验操作,与表中结论相符的预期现象.
| 实验操作 | 预期现象 | 结论 |
| 步骤1:取少量固体于试管中,滴加适量的稀盐酸或稀硫酸 | 不产生气泡 | 假设2成立 |
| 步骤2:另取少量固体于另一支试管中,加足量的水溶解,滴加适量的氯化钡溶液 | 不产生白色沉淀 |
17.农业生产常用到下列化肥.属于钾肥的是( )
| A. | CO(NH2)2 | B. | NaNO3 | C. | NH4Cl | D. | K2SO4 |
7.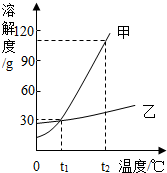 甲、乙两种固体物质的溶解度曲线如图所示,下列说法错误的是( )
甲、乙两种固体物质的溶解度曲线如图所示,下列说法错误的是( )
 甲、乙两种固体物质的溶解度曲线如图所示,下列说法错误的是( )
甲、乙两种固体物质的溶解度曲线如图所示,下列说法错误的是( )| A. | t1℃时,甲、乙的溶解度相等 | |
| B. | 甲、乙中,甲的溶解度受温度的影响较大 | |
| C. | t2℃时,甲的溶解度大于乙的溶解度甲 | |
| D. | t2℃时,在100 g水中加入90 g甲,形成饱和溶液 |