题目内容
20. 学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液摆放在实验桌上,让同学们区分.下面是“雄鹰小组”同学们的探究过程:
学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液摆放在实验桌上,让同学们区分.下面是“雄鹰小组”同学们的探究过程:[讨论交流]李壮:区分两种物质的原理是:依据物质的性质,选择一种试剂与两种物质混合,产生两种不同的现象.大家据此来说一说,区分这两种溶液应选用哪种试剂,并说明理由.
王志:我认为可以选择稀盐酸,理由是稀盐酸与碳酸钠反应有气泡产生,稀盐酸与氢氧化钙反应无明显现象.
马凌:我选择的是碳酸钠溶液,理由是碳酸钠与氢氧化钙反应生成沉淀.
张云:马凌,你说的我没有听懂,你能再给我讲一遍吗?在大家的帮助下,张云不但弄明白了,还选出了其他两种溶液,如氯化钙溶液和氢氧化钙溶液,最后得到大家的赞许.
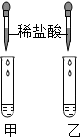
[实验探究]大家按照王志的方案进行了如图所示的实验:
(1)实验中同学们根据观察到的现象,判断出甲试管中原溶液为碳酸钠溶液,乙试管中原溶液为石灰水.
(2)大家对乙试管中现有溶液的溶质成分产生了探究兴趣.马凌经过认真思考后,又选择碳酸钠溶液作为检验试剂,进行了如下实验:
①马凌从乙试管中取少量溶液加入到另一支新试管中,再向此新试管中加入足量的碳酸钠溶液,观察到只有白色沉淀生成.于是,他得出结论:“溶液中的溶质有氢氧化钙.”但组长李壮对这个结论产生质疑,理由是Na2CO3+CaCl2=CaCO3↓+2NaCl(用化学方程式表示).
②大家讨论完李壮的质疑,制定出测定溶液酸碱度的方法来验证他的质疑,并查阅资料得知氯化钙溶液呈中性,大家都鼓励张云来做实验.张云测出乙试管中剩余溶液的pH=7(填“>”、“<”或“=”),证实了马凌的结论是错误的.
[反思评价]判断反应后溶液中溶质的成分,除要考虑生成物外,还需考虑反应物是否有剩余.探究活动结束了,同学们充分体验到合作探究的乐趣和学习成功的喜悦!
分析 【讨论交流】根据碳酸钠和氢氧化钙反应生成白色的碳酸钙沉淀进行分析;
根据钙离子和碳酸根离子会生成碳酸钙沉淀进行分析;
【实验探究】(2)①根据氢氧化钙和盐酸反应生成氯化钙,氯化钙和碳酸钠会生成碳酸钙沉淀和氯化钠进行分析;
②根据氢氧化钙属于碱,溶液显碱性,pH值大于7进行分析;
【反思评价】根据物质之间发生反应时的量进行分析.
解答 解:【讨论交流】碳酸钠和氢氧化钙反应生成白色的碳酸钙沉淀,所以选择碳酸钠溶液的理由是:碳酸钠和氢氧化钙反应会生成白色沉淀;
钙离子和碳酸根离子会生成碳酸钙沉淀,所以还可以选择的两种溶液是氯化钙溶液和氢氧化钙溶液;
【实验探究】(2)①氢氧化钙和盐酸反应生成氯化钙,氯化钙和碳酸钠会生成碳酸钙沉淀和氯化钠,所以化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl;
②氢氧化钙属于碱,溶液显碱性,pH值大于7,所以张云测出乙试管中剩余溶液的pH=7,证实了马凌的结论是错误的;
【反思评价】判断反应后溶液中溶质的成分,除要考虑生成物外,还需考虑反应物是否有剩余.
故答案为:【讨论交流】碳酸钠和氢氧化钙反应会生成白色沉淀;氯化钙,氢氧化钙;
【实验探究】(2)①Na2CO3+CaCl2=CaCO3↓+2NaCl;②=;
【反思评价】反应物是否有剩余.
点评 本题考查了常见物质的性质,在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中所给的知识进行解答.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
8.由一氧化碳和二氧化碳两种气体组成的混合气体,经分析知混合气体的含碳量为30%,则一氧化碳和二氧化碳在混合气体中的质量比为( )
| A. | 10:8 | B. | 7:11 | C. | 7:33 | D. | 33:7 |
5.下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A. | O | B. | He | C. | N2 | D. | CO |
12.小杰和小敬学习了碳单质的化学性质后,知道碳与氧气反应能够生成CO或CO2.于是两人联想到木炭粉与氧化铜发生的反应可能有:
①2CuO+C $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑
②CuO+C$\frac{\underline{\;高温\;}}{\;}$Cu+CO↑他们想来验证自己的想法,请你同他们一起进行探究.
【猜想与假设】木炭粉与氧化铜反应生成的产物有三种可能:
(1)产物是铜和一氧化碳;(2)产物是铜和二氧化碳;(3)产物是铜和一氧化碳、二氧化碳.
【设计方案】
(1)检验产物中是否有CO2的方法是Ca(OH)2+CO2═CaCO3↓+H2O;
(2)如何检验产物中是否存在CO,两人查找了资料:CO的特征反应是CO能使黄色溶液氯化钯变蓝.
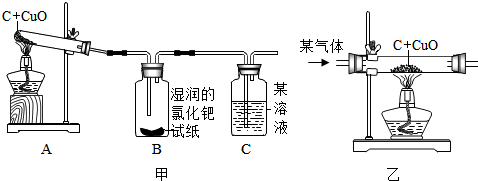
【实验与结论】设计的实验装置(如甲图):
实验报告
【反思与评价】
(1)实验结束时,为防止Cu被氧化,必须先停止加热,待Cu冷却后再将试管口的胶塞取下,因此,若没有B安全瓶,可能导致的后果是液体倒吸入试管把试管炸裂;
(2)根据实验结论,从环保角度考虑,上述装置C后应添加的装置是酒精灯.
【拓展与交流】如果用乙图装置代替甲图中的A装置,这样既可以排尽试管中的空气,又能将反应的气体产物都“赶”出来,某气体应是N2.
①2CuO+C $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑
②CuO+C$\frac{\underline{\;高温\;}}{\;}$Cu+CO↑他们想来验证自己的想法,请你同他们一起进行探究.

【猜想与假设】木炭粉与氧化铜反应生成的产物有三种可能:
(1)产物是铜和一氧化碳;(2)产物是铜和二氧化碳;(3)产物是铜和一氧化碳、二氧化碳.
【设计方案】
(1)检验产物中是否有CO2的方法是Ca(OH)2+CO2═CaCO3↓+H2O;
(2)如何检验产物中是否存在CO,两人查找了资料:CO的特征反应是CO能使黄色溶液氯化钯变蓝.
【实验与结论】设计的实验装置(如甲图):
实验报告
| 实验现象 | 实验结论 |
| ①A中固体由黑色变为红色 ②若B中黄色试纸变蓝 ③若C中澄清石灰水变浑浊 | ①有铜生成 ②有CO生成 ③有CO2生成 |
(1)实验结束时,为防止Cu被氧化,必须先停止加热,待Cu冷却后再将试管口的胶塞取下,因此,若没有B安全瓶,可能导致的后果是液体倒吸入试管把试管炸裂;
(2)根据实验结论,从环保角度考虑,上述装置C后应添加的装置是酒精灯.
【拓展与交流】如果用乙图装置代替甲图中的A装置,这样既可以排尽试管中的空气,又能将反应的气体产物都“赶”出来,某气体应是N2.
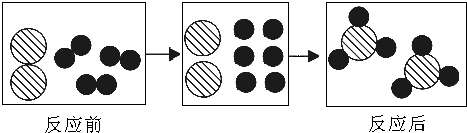
9.化学现象中有许多“相等”,下列有关“相等”的说法,错误的是( )
| A. | 原子中的质子数和核外电子数一定相等 | |
| B. | 反应前后各原子总数相等 | |
| C. | 50mL酒精和50mL水混合,其体积与混合前二者的体积之和一定相等 | |
| D. | 化学反应前后,参加化学反应的各物质的质量总和与生成的各物质的质量总和一定相等 |

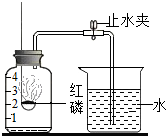 已知空气的主要成分是氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验.实验装置如图所示:
已知空气的主要成分是氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验.实验装置如图所示: