题目内容
10.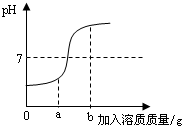 在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示.
在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示.(1)该反应的化学方程式为HCl+NaOH═NaCl+H2O;
(2)该实验操作是将氢氧化钠溶液滴加到另一种溶液中;
(3)当加入溶液的质量为ag时,所得溶液中的溶质为(写化学式)HCl、NaCl;
(4)当加入溶液的质量为bg时,向所得溶液中滴加酚酞溶液,溶液呈红色.
分析 (1)氢氧化钠和盐酸反应能生成氯化钠和水;
(2)盐酸显酸性,pH小于7,氢氧化钠溶液显碱性,pH大于7;
(3)当盐酸过量时,盐酸和氢氧化钠反应后的溶液中含有氯化氢、氯化钠;
(4)显碱性的溶液能使酚酞试液变红色.
解答 解:(1)稀盐酸和氢氧化钠溶液反应的化学方程式为:NaOH+HCl=NaCl+H2O.
(2)开始时溶液的pH小于7,说明是把氢氧化钠溶液滴加到稀盐酸中.故填:氢氧化钠溶液.
(3)当加入溶液的质量为ag时,溶液的pH小于7,说明盐酸过量,所得溶液中的溶质为氯化氢和氯化钠.故填:HCl、NaCl.
(4)当加入溶液的质量为bg时,溶液的pH大于7,溶液显碱性,显碱性的溶液能使酚酞试液变红色.故填:红色.
点评 本题主要考查溶液的酸碱性和pH之间的关系,同时考查了化学方程式的书写方面的知识,书写化学方程式时要注意遵循质量守恒定律.

练习册系列答案
相关题目
1.某校化学兴趣小组的同学在探究酸碱中和反应时,将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中,反应的化学方程式是:H2SO4+2NaOH═Na2SO4 +2H2O.未观察到明显现象,部分同学对实验产生了疑问:反应后溶液中溶质是什么呢?
【提出猜想】针对疑问,小明同学作出如下猜想:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
小华同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的是猜想四.
【实验探究】同学们对剩余的猜想进行了探究:
(1)取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,学习小组的同学设计了三套实验方案:
【实验结论】经过实验探究,大家一致认为猜想二是正确的.
【实验反思】写出方案一的化学方程式:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
三个方案中有一个方案是错误的,原因是BaCl2与Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
【提出猜想】针对疑问,小明同学作出如下猜想:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
小华同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的是猜想四.
【实验探究】同学们对剩余的猜想进行了探究:
(1)取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,学习小组的同学设计了三套实验方案:
| 实验方案 | 取少量烧杯中溶液 | 实验现象 | 实验结论 |
| 方案一 | 加入Na2CO3溶液 | 有气泡产生 | 溶液中有H2SO4 |
| 方案二 | 滴加紫色石蕊溶液 | 溶液变红 | 溶液中有H2SO4 |
| 方案三 | 加入BaC12溶液 | 有白色沉淀生成 | 溶液中有H2SO4 |
【实验反思】写出方案一的化学方程式:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
三个方案中有一个方案是错误的,原因是BaCl2与Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
18.我校学生进行了如图所示的实验.

(1)甲实验中滴加稀盐酸后,可观察到的现象是溶液变无色,证明两者确实发生了反应.
(2)乙实验中反应的方程式CO2+2NaOH═Na2CO3+H2O.
(3)丙实验中试管内有白色沉淀产生.
(4)实验结束后,同学们将甲、乙、丙三个实验的废液倒人同一个干净的废液缸中,最终看到废液浑浊并呈红色,由此说明废液中含有碳酸钙,一定不含有盐酸.
【提出问题】废液中究竟含有哪些物质?
【交流讨论】
①一定含有的物质:碳酸钙、指示剂、水和氯化钠.
②还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有如下猜想.
小方认为:只有碳酸钠
小丽认为:只有氢氧化钙
小云认为:是氢氧化钠和碳酸钠
小新认为:只有氢氧化钠
你认为还可能是:氢氧化钠和氢氧化钙.
【实验设计】小斌想用氯化钙溶液来验证小方的猜想.查阅资料获悉氯化钙溶液呈中性,并设计如下实验.请你将小斌的实验设计补充完整.
【反思拓展】在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑反应物是否有剩余.

(1)甲实验中滴加稀盐酸后,可观察到的现象是溶液变无色,证明两者确实发生了反应.
(2)乙实验中反应的方程式CO2+2NaOH═Na2CO3+H2O.
(3)丙实验中试管内有白色沉淀产生.
(4)实验结束后,同学们将甲、乙、丙三个实验的废液倒人同一个干净的废液缸中,最终看到废液浑浊并呈红色,由此说明废液中含有碳酸钙,一定不含有盐酸.
【提出问题】废液中究竟含有哪些物质?
【交流讨论】
①一定含有的物质:碳酸钙、指示剂、水和氯化钠.
②还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有如下猜想.
小方认为:只有碳酸钠
小丽认为:只有氢氧化钙
小云认为:是氢氧化钠和碳酸钠
小新认为:只有氢氧化钠
你认为还可能是:氢氧化钠和氢氧化钙.
【实验设计】小斌想用氯化钙溶液来验证小方的猜想.查阅资料获悉氯化钙溶液呈中性,并设计如下实验.请你将小斌的实验设计补充完整.
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置. | 小方的猜想正确. |
5.呼吸面具中“氧气再生剂”的主要成分是淡黄色固体过氧化钠(Na2O2),使用后变成白色固体.某兴趣小组对白色固体的成分进行探究:
【查阅资料】
2Na2O2+2CO2═2Na2CO3+O2
2Na2O2+2H2O═2NaOH+O2↑
【提出猜想】根据呼出的气体中含有较多的二氧化碳和水蒸气.对白色固体作出如下猜想:猜想Ⅰ:氢氧化钠 猜想Ⅱ:碳酸钠 猜想Ⅲ:氢氧化钠和碳酸钠
【实验验证】
【得出结论】猜想Ⅲ成立
【拓展应用】“氧气再生剂”的保存方法是密封存放干燥处.
【查阅资料】
2Na2O2+2CO2═2Na2CO3+O2
2Na2O2+2H2O═2NaOH+O2↑
【提出猜想】根据呼出的气体中含有较多的二氧化碳和水蒸气.对白色固体作出如下猜想:猜想Ⅰ:氢氧化钠 猜想Ⅱ:碳酸钠 猜想Ⅲ:氢氧化钠和碳酸钠
【实验验证】
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品溶于水,加入适量氯化钙溶液 | 产生白色沉淀 | 该反应的化学方程式为 Na2CO3+CaCl2=2NaCl+CaCO3↓ |
| (2)将上述反应后的混合物过滤取滤液加入 无色酚酞试液 | 无色变红色 | 证明猜想Ⅲ正确 |
【拓展应用】“氧气再生剂”的保存方法是密封存放干燥处.
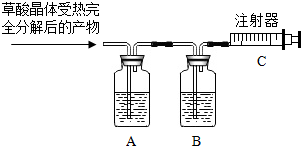 有些晶体按比例带有一定量的结晶水,带有结晶水的晶体在一定温度下会脱去结晶水.草酸晶体(H2C2O4•xH2O)在常温下是一种无色透明晶体.草酸晶体受热时分解的化学方程式为:H2C2O4•xH2O$\frac{\underline{\;\;△\;\;}}{\;}$(x+1)H2O+CO2↑+CO↑
有些晶体按比例带有一定量的结晶水,带有结晶水的晶体在一定温度下会脱去结晶水.草酸晶体(H2C2O4•xH2O)在常温下是一种无色透明晶体.草酸晶体受热时分解的化学方程式为:H2C2O4•xH2O$\frac{\underline{\;\;△\;\;}}{\;}$(x+1)H2O+CO2↑+CO↑