题目内容
14. 氯化钠、硝酸钾、硒酸镉的溶解度曲线如图所示,据图回答:
氯化钠、硝酸钾、硒酸镉的溶解度曲线如图所示,据图回答:(1)溶解度受温度变化影响最大的是硝酸钾;
(2)t℃时,将25g硒酸镉加入50g水中,完全溶解后,恰好得到饱和溶液,要进一步提高该溶液的溶质质量分数,可进行的操作是降低温度再加入硒酸镉;
(3)硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是降温结晶.
分析 根据题目信息和溶解度曲线可知:硝酸钾、氯化钠两种固体物质的溶解度,都是随温度升高而增大,而硒酸镉的溶解度随温度的升高而减少;溶解度受温度变化影响最大的是硝酸钾;t℃时,硒酸镉的溶解度是50g,因此将25g硒酸镉加入50g水中,完全溶解后,恰好得到饱和溶液,要进一步提高该溶液的溶质质量分数,可进行的操作是:降低温度再加入硒酸镉;硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是降温结晶,因为硝酸钾的溶解度受温度影响变化最大.
解答 解:(1)由溶解度曲线可知:硝酸钾、氯化钠两种固体物质的溶解度,都是随温度升高而增大,溶解度受温度变化影响最大的是硝酸钾;故答案为:硝酸钾;
(2)t℃时,硒酸镉的溶解度是50g,因此将25g硒酸镉加入50g水中,完全溶解后,恰好得到饱和溶液,要进一步提高该溶液的溶质质量分数,可进行的操作是:降低温度再加入硒酸镉;故答案为:50;降低温度再加入硒酸镉;
(3)硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是降温结晶,因为硝酸钾的溶解度受温度影响变化最大;故答案为:降温结晶;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液结晶的方法等,本考点主要出现在选择题和填空题中.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
1.实验中学课外活动小组在测定由氯化钠和硫酸钠形成混合物的组成时,进行了以下实验:取20g混合物全部溶于水,将得到的溶液等分为4份,然后分别加入一定量未知质量分数的氯化钡溶液,实验数据见表:
请计算:
(1)未知氯化钡溶液的质量分数为多少?
(2)原混合物中硫酸钠的质量分数是多少?
| 第一份 | 第二份 | 第三份 | 第四份 | |
| 加入氯化钡溶液质量(g) | 15 | 20 | 25 | 30 |
| 反应得到沉淀的质量(g) | 1.40 | 1.87 | 2.33 | 2.33 |
(1)未知氯化钡溶液的质量分数为多少?
(2)原混合物中硫酸钠的质量分数是多少?
2.下列关于化学实验操作或实验思路正确的是( )
| A. | 用稀盐酸洗涤试管内壁的油污 | |
| B. | 往某溶液中滴加BaCl2溶液和稀硝酸,产生白色沉淀,则该溶液中一定含有SO42- | |
| C. | 稀释浓硫酸时,把水沿烧杯壁慢慢注入盛浓硫酸的烧杯中并不断搅拌 | |
| D. | 在淀粉溶液中加入适量“加碘食盐”发现不变蓝,说明“加碘食盐”中不含单质碘 |
2.生活中常遇到“碘盐”“高钙牛奶”“铁强化酱油”等商品,这里的“碘、钙、铁”是指( )
| A. | 单质 | B. | 原子 | C. | 分子 | D. | 元素 |
9.钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将125g盐酸分成5等份,逐次加到用50片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如下.请根据有关信息回答问题.
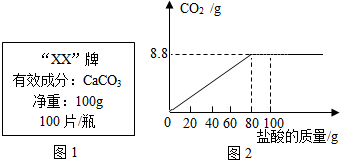
(1)该品牌补钙药剂中CaCO3的质量分数是40%,a的数值为35.
(2)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数).
(3)求恰好完全反应时所得溶液的溶质质量分数(写出计算过程,计算结果保留一位小数).

| 第1次 | 第3次 | 第4次 | |
| 加入盐酸的质量(g) | 25 | 25 | 25 |
| 剩余固体的质量(g) | 45 | a | 30 |
(2)求该盐酸中溶质的质量分数(写出计算过程,计算结果保留一位小数).
(3)求恰好完全反应时所得溶液的溶质质量分数(写出计算过程,计算结果保留一位小数).
6.下列用品有效成分的化学式及用途对应正确的是 ( )
| A、小苏打 | B、硝酸钾 | C、葡萄糖 | D、烧碱 | |
| 用品 |  |  |  |  |
| 有效成分 | Na2CO3 | KNO3 | C6H12O6 | NaOH |
| 用途 | 做发酵粉 | 做复合肥 | 做调味剂 | 治疗胃酸过多 |
| A. | A | B. | B | C. | C | D. | D |
