题目内容
11.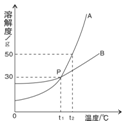 根据如图中a、b两种物质的溶解度曲线,回答下列问题:
根据如图中a、b两种物质的溶解度曲线,回答下列问题:(1)把t2℃时等质量A、B两物质的饱和溶液降低到t1℃,析出晶体较多的是A.
(2)t2℃时,将90gA物质投入到100g水中,得到A物质的饱和(填“饱和”或“不饱和”) 溶液,此时溶液的质量是150g.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)根据图示可以看出,A物质的溶解度随温度的升高变化明显,故把t2℃时等质量A、B两物质的饱和溶液降低到t1℃,析出晶体较多的是A,故填:A.
(2)t2℃时,A物质的溶解度为50g,故将90gA物质投入到100g水中,只能溶解50g,得到A物质的饱和溶液,此时溶液的质量是150g,故填:饱和;150.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
16.将浓硫酸长时间放在敞口容器中,硫酸的质量分数会变小,这是因为浓硫酸具有吸水性;将浓硫酸滴在纸上或布上时,纸或布的颜色会变黑,这是浓硫酸使它们碳化(即脱水作用)的缘故,因为浓硫酸具有强烈的脱水性.
3.下列各组物质中,在通常情况下不能发生化学反应的是( )
| A. | 铁与硫酸铜溶液 | B. | 氢氧化镁与稀盐酸 | ||
| C. | 碳酸钠与稀硫酸 | D. | 氯化钠和和稀硫酸 |
20.10克镁铝合金与足量稀硫酸充分反应后生成1克氢气,则合金中镁铝的质量比为( )
| A. | 2:1 | B. | 3:2 | C. | 2:3 | D. | 1:2 |
 小明想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供一瓶稀盐酸和必要的仪器.
小明想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供一瓶稀盐酸和必要的仪器.
 小明同学将12.5g含杂质石灰石样品与足量稀盐酸相混合,充分反应,如图是生成气体的质量(m)随时间(t)变化的曲线.
小明同学将12.5g含杂质石灰石样品与足量稀盐酸相混合,充分反应,如图是生成气体的质量(m)随时间(t)变化的曲线.