题目内容
1.甲醛(CH2O)的水溶液中氢元素的质量分数为10%,则碳元素的质量分数为10%,甲醛的质量分数为25%.分析 由甲醛和水的化学式可知,二者中氢元素与氧元素的质量比均为(1×2):16=1:8;可分析出水溶液中氧元素的质量分数,并进一步计算出碳元素的质量分数和甲酸的质量分数.
解答 解:由甲醛和水的化学式可知,二者中氢元素与氧元素的质量比均为(1×2):16=1:8;已知甲醛(CH2O)的水溶液中氢元素的质量分数为10%,则其中氧元素的质量分数为80%,则碳元素的质量分数为:1-10%-80%=10%;甲醛的相对分子质量为:12+1×2+16=30.设水溶液中甲醛的质量分数为x,则
$\frac{10%}{x}=\frac{12}{30}$,x=25%.
故填:10%;25%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
9.下列关于水的说法不正确的是( )
| A. | 水是常用来溶解其它物质 | B. | 自然界中的水都是混合物 | ||
| C. | 过滤可以除去天然水中的各种杂质 | D. | 长期饮用蒸馏水无益于人体的健康 |
16.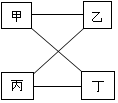 如表提供的四组物质符合如图所示相连物质在一定条件下可以发生反应的是( )
如表提供的四组物质符合如图所示相连物质在一定条件下可以发生反应的是( )
 如表提供的四组物质符合如图所示相连物质在一定条件下可以发生反应的是( )
如表提供的四组物质符合如图所示相连物质在一定条件下可以发生反应的是( )| 甲 | 乙 | 丙 | 丁 | |
| A | NaOH | HCl | Cu | AgNO3 |
| B | CO2 | Ca(OH)2 | Na2CO3 | CaCl2 |
| C | KOH | BaCl2 | K2CO3 | HCl |
| D | CuSO4 | BaCl2 | Na2CO3 | Ba(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
6.下列各组物质中,前者不是后者溶质的是( )
| A. | 氯化钠、食盐水 | B. | 碘、碘酒 | C. | 氯化氢、盐酸 | D. | 氧化钙、石灰水 |
13.10℃时,50克水里最多溶解甲物质10克,20℃时100克水里最多溶解乙物质20克,且甲、乙两物质的溶解度都随温度的升高而增大.则在15℃时甲、乙两物质的溶解度的关系为( )
| A. | 甲>乙 | B. | 甲=乙 | C. | 甲<乙 | D. | 无法确定 |
10.下列各组物质,只用一种试剂(括号内物质)及相互之间的反应不能鉴别开来的是( )
| A. | 固体:食盐、硝酸铵、烧碱 (水) | |
| B. | 固体:硫酸铜、熟石灰、碳酸钙(稀盐酸) | |
| C. | 溶液:纯碱、食盐、盐酸 (酚酞试液) | |
| D. | 溶液:氯化钠、氯化钾、硫酸钾(硝酸银溶液) |
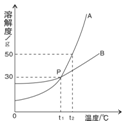 根据如图中a、b两种物质的溶解度曲线,回答下列问题:
根据如图中a、b两种物质的溶解度曲线,回答下列问题: