题目内容
6.实验室现有如图1仪器.回答下列问题.
(1)标号②的仪器名称是锥形瓶;
(2)实验室用高锰酸钾制取氧气:
a.组装发生装置时可以选择所给仪器中的①、⑤、⑧和⑦;该实验中还要用到棉花,棉花的作用是
防止高锰酸钾进入导管.
b.发生反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室制取制取二氧化碳气体,若要制得2.2g二氧化碳,则反应的碳酸钙的质量为5g;同学们设计了图2所示的装置来收集二氧化碳,则二氧化碳应该从a(填“a”或“b”)端通入,验满的方法是把燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明已经收集满.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
为了防止高锰酸钾进入导管,通常在试管口塞一团棉花;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能够溶于水,密度比空气大,不能燃烧,不支持燃烧.
解答 解:(1)标号②的仪器名称是锥形瓶.
故填:锥形瓶.
(2)a.组装发生装置时可以选择所给仪器中的①、⑤、⑧和⑦;
该实验中还要用到棉花,棉花的作用是防止高锰酸钾进入导管.
b.发生反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
故填:⑦;防止高锰酸钾进入导管;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)解:设若要制得2.2g二氧化碳,需要的碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 2.2g
$\frac{100}{x}$=$\frac{44}{2.2g}$,
x=5g,
设计了图2所示的装置来收集二氧化碳,由于二氧化碳密度比空气大,则二氧化碳应该从a端通入,验满的方法是:把燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明已经收集满.
故填:5;a;把燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明已经收集满.
点评 本题主要考查仪器的用途、反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案| A. | 质量很小 | B. | 体积很小 | C. | 之间有间隔 | D. | 不断运动 |
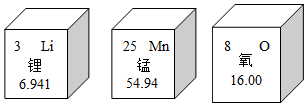
| A. | 锂是非金属元素 | B. | 锰的核内质子数为25 | ||
| C. | 氧的相对原子质量是16.00 | D. | 原子核外电子数Li>Mn>O |
| A. | -3 | B. | +1 | C. | +3 | D. | +5 |
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.54 | 3.08 | 4.4 | m |
(2)上表中m的数值是4.4;
(3)若将 15克这种石灰石矿完全反应最多能产生多少克二氧化碳?
(4)试计算15克这种石灰石矿中碳酸钙的质量(该题写出计算步骤)

 某同学对教材中硫在氧气中燃烧的实验进行了改进.具体操作是:在燃烧匙中放少量硫粉,点燃后伸入充满氧气且底部有较多量水的集气瓶中(如图所示).观察到实验现象后,立即将燃烧匙浸入瓶内水中.请分析实验过程,回答下列问题:
某同学对教材中硫在氧气中燃烧的实验进行了改进.具体操作是:在燃烧匙中放少量硫粉,点燃后伸入充满氧气且底部有较多量水的集气瓶中(如图所示).观察到实验现象后,立即将燃烧匙浸入瓶内水中.请分析实验过程,回答下列问题: 甲、乙、丙是初中化学常见的物质,甲在一定条件下分解成乙和丙,乙是最常用的氧化物.三种物质转化关系如图所示(部分反应物、生成物和反应条件已略去).若甲、乙组成元素相同,则丙是氧气(或O2).从微观角度解释,甲、乙化学性质不同的原因是分子结构不同(合理即可).
甲、乙、丙是初中化学常见的物质,甲在一定条件下分解成乙和丙,乙是最常用的氧化物.三种物质转化关系如图所示(部分反应物、生成物和反应条件已略去).若甲、乙组成元素相同,则丙是氧气(或O2).从微观角度解释,甲、乙化学性质不同的原因是分子结构不同(合理即可).