题目内容
16. 某研究性学习小组的同学为探究金属镍(Ni,银白色金属)和铜的活动性顺序,进行了一系列实验活动.请你一起参与他们的活动,并回答有关问题.
某研究性学习小组的同学为探究金属镍(Ni,银白色金属)和铜的活动性顺序,进行了一系列实验活动.请你一起参与他们的活动,并回答有关问题.探究活动一、金属镍和铜的活动性顺序
| 实验方案 | 实验现象 | 实验结论 |
| 将金属镍加入到盛有硫酸铜溶液的试管中 | 溶液的颜色变浅,有红色固体析出 | 镍比铜的金属活动性强 |
实验过程中,小组同学还发现试管中有无色气体产生的“异常”现象,十分好奇,于是继续进行探究活动.
探究活动二、无色气体的成分是什么?
【猜想假设】A.氢气 B.氧气 C.二氧化硫 D.二氧化碳 E.一氧化碳
【分析推理】小明认为无色气体不可能是二氧化碳或一氧化碳,理由是反应物中不含碳元素,化学反应前后元素种类不变.
小红根据二氧化硫能够形成酸雨的事实,推测二氧化硫能溶于水,且水溶液应该呈酸性能使指示剂变色小组同学认为小红的观点合理,于是将收集到到气体收入紫色石蕊溶液溶液中,发现溶液不变色,证明无色气体不是二氧化硫.
综上所述,小组同学认为,无色气体可能是氢气,或者氧气.
【设计方案】为确定气体成分,小组同学设计了如下实验方案:
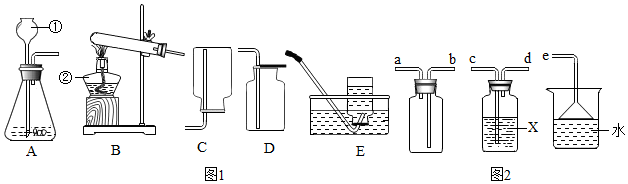
用如图所示装置进行实验,先检验气体纯度,然后将燃着的木条放在尖嘴处,发现气体燃烧并发出淡蓝色火焰,证明无色气体可能是氢气.
该实验方案中浓硫酸的作用是除去气体中的水分.
【评价与反应】小组同学认为,还可以补充一个实验,验证无色气体中含有氢元素,从而进一步证明无色气体可能是氢气.他们应补充的实验是在点燃气体的火焰上方罩一个干冷的烧杯,烧杯内壁产生水珠.
分析 探究活动一、将金属镍加入到盛有硫酸铜溶液的试管中,由实验结论中“镍比铜的金属活动性强”可知镍可把铜从硫酸铜溶液中置换出来去分析;
【分析推理】
根据质量守恒定律:化学反应前后 元素种类不变去分析;
【设计方案】
从氢气是可燃性气体,浓硫酸具有吸水性去分析;
【评价与反应】
根据质量守恒定律,化学反应前后元素的种类不变.要验证气体中含有氢元素,将其点燃,看生成物中是否有水生成.
解答 解:探究活动一、将金属镍加入到盛有硫酸铜溶液的试管中,由实验结论中“镍比铜的金属活动性强”可知镍可把铜从硫酸铜溶液中置换出来,其反应的化学方程式为:Ni+CuSO4=NiSO4+Cu;由于有铜生成,所以会有红色的物质出现;
【分析推理】
由于反应物中不含碳元素,根据质量守恒定律:化学反应前后 元素种类不变;可知不可能是二氧化碳或一氧化碳;由题意可知:二氧化硫能溶于水,且水溶液应该呈酸性能使紫色石蕊溶液变红;
【设计方案】
由题目中结论该气体可能是氢气,由于氢气是可燃性气体,所以使用时要检验氢气的纯度;浓硫酸具有吸水性,可除去气体中的水分;
【评价与反应】
根据质量守恒定律,化学反应前后元素的种类不变.要验证气体中含有氢元素,可在点燃气体的火焰上方罩一个干冷的烧杯,如果烧杯内壁产生水珠,说明生成了水,水是由氢元素和氧元素组成的,从而证明反应物中含有氢元素;
故答案为:在点燃气体的火焰上方罩一个干冷的烧杯,烧杯内壁产生水珠.
答案:探究活动一、红; Ni+CuSO4=NiSO4+Cu;
【分析推理】反应物中不含碳元素,化学反应前后 元素种类不变;紫色石蕊溶液
【设计方案】检验气体纯度; 除去气体中的水分;
【评价与反应】在点燃气体的火焰上方罩一个干冷的烧杯,烧杯内壁产生水珠.
点评 要会利用金属活动顺序表设计实验,去验证金属的还原性强弱.前边的金属会把后边的金属从其盐溶液中置换出来.灵活运用质量守恒定律等.

问题一:黑色固体是什么?
【交流讨论】同学们结合实验现象和对高锰酸钾及其分解产物的了解.进行分析判断.
| 判断 | 依据 |
| 不是KMNO4 | KMNO4能溶于水形成紫红色溶液 |
| 不是K2MnO4(填化学式) | 冲洗试管时出现深绿色溶液,说明该物质能溶于水 |
| 是MnO2 | 其他实验用过MnO2,知道它是不溶于水的黑色固体 |
问题二:用什么洗掉MnO2?
【交流讨论】MnO2与BaCO3、Mg(OH)2、Fe2O3、P2O5、Cu中的某一种物质组成最相近,理由是都是金属氧化物.这种物质能与稀盐酸反应,化学方程式为Fe2O3+6HCl=3H2O+2FeCl3,由此推测MnO2也能与稀盐酸反应.
【实验验证】向未洗净的试管中加入稀盐酸,黑色固体没有变化.
【交流讨论】实验说明同一类物质的化学性质不一定相同.MnO2有什么化学性质,用什么试剂清洗呢?同学们请教老师后决定用草酸(H2C2O4)溶液试一试.
【实验验证】向未洗净的试管中加入草酸溶液,黑色固体果然被除去,同时发现产生许多气泡.
问题三:生产了什么气体?
【交流讨论】化学变化过程中元素不变,因为质量守恒定律,反应物中的元素只有碳、氢、氧,所以产生的气体可能为CO2、CO、H2、O2等.
【实验验证】经检验,产生的气体是CO2,检验CO2气体的操作和现象是:将气体通入澄清石灰水中,石灰水变浑浊,说明该气体是二氧化碳.
【反思提高】以上探究活动中,清除试管内壁附着的难溶物的思路是:先了解其物理性质,尤其是否溶于水,再了解其化学性质,然后选择合适试剂进行清洗.
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
【实验验证】
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想二不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 | 先无变化后产生气泡 | 猜想三成立 |
(1)氢化钙与水反应的化学方程式为CaH2+2H2O=2H2↑+Ca(OH)2;
(2)若向NH4Cl的溶液中加一定量CaH2,充分反应,产生的气体是氢气、氨气;
(3)登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是携带安全.
| A. | 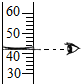 量取液体 | B. | 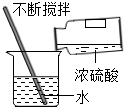 浓硫酸稀释 浓硫酸稀释 | C. |  CO2的验满 | D. | 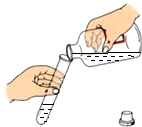 液体的倾倒 |
【方法探究】为了除去二氧化碳气体中混有的少量一氧化碳,小明设计了三种方案.
| 实验方案 | |
| 方案A |  |
| 方案B | 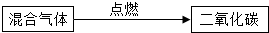 |
| 方案C | 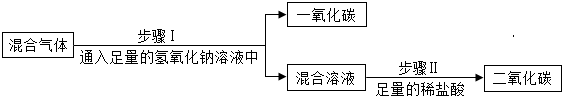 |
【方法提炼】上述两种合理方案体现了物质除杂的不同思路:
思路一:将杂质直接转化为所需物质;
思路二:将所需物质转化为中间物质,在将中间物质转化为所需物质.
【方法运用】
运用思路一:除去氯化镁粉末中混有的少量氯化钡,先加足量的水溶解,再向溶液中加入适量的硫酸镁溶液,过滤、蒸发,即得氯化镁固体.
运用思路二:除去氯化镁粉末中混有的少量氯化钡、氯化钠和硫酸钾.
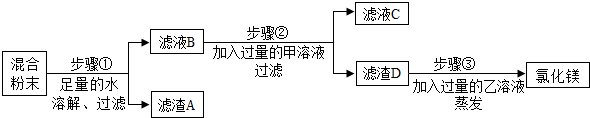
步骤①中反应的化学方程式是BaCl2+K2SO4═BaSO4↓+2KCl,滤液B中一定含有的溶质是氯化钾、氯化钠、氯化镁;
步骤②中反应的化学方程式是2NaOH+MgCl2=Mg(OH)2↓+2NaCl,滤液C中一定含有的阴离子是氯离子和氢氧根离子;
步骤③中乙溶液是HCl(填化学式)溶液.
| A. | Ca(H2PO4)2 | B. | K2CO3 | C. | CO(NH2)2 | D. | KNO3 |