题目内容
8.石灰石的主要成分为CaCO3,可用于制生石灰.我市某地出产一种石灰石,其中CaCO3的质量分数为80%,试回答下列问题:(其余杂质不参与反应)(1)CaCO3中钙元素的质量分数为40%.
(2)100吨该石灰石中含钙元素的质量为32吨,经过充分冶炼,最多可生产含CaO 96%的生石灰46.7吨(最后一空保留两位小数).
分析 (1)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数解答;
(2)根据碳酸钙的质量求出含CaO 96%的生石灰含即可.
解答 解:
(1)CaCO3中钙元素的质量分数为$\frac{40}{40+12×16×3}$×100%=40%;
(2)100吨该石灰石中含钙元素的质量为100t×80%×40%=32t
设可生产含CaO 96%的生石灰的质量为x
CaCO3 $\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 56
100t×80% x×96%
$\frac{100}{100t×80%}=\frac{56}{x×96%}$
x≈46.7t
答案:(1)40%;
(2)32;46.7.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
18.实验室提供以下药品和仪器,请回答:
药品:氯酸钾、高锰酸钾、大理石、二氧化锰、稀盐酸、过氧化氢溶液.
仪器:图1
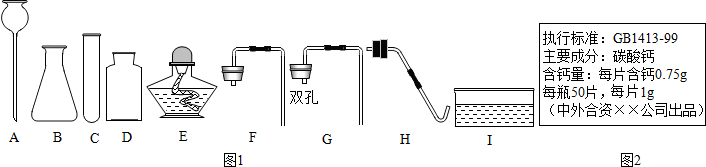
(1)请从图1仪器中选择适当的仪器组装一套实验室制取二氧化碳的装置(包括发生装置和收集装置):ABGD,写出反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)如果选用碳酸钠粉末和稀盐酸来制取二氧化碳,为了控制反应速率,应对该气体发生装置如何改进?(可另增仪器)分液漏斗.
(3)利用(1)中装置和以上药品还可以制取氢气,选择的药品是:锌粒和稀硫酸.
(4)某钙片的标签如图2,且知钙片中只有碳酸钙中含有钙元素,但人们发现其中的含钙量是不符合事实的;某实验小组为测定其真实的含钙量做了如下实验,每次取10片钙片放入已称量的含足量盐酸的烧杯中,充分反应后称取烧杯和剩余物质的总质量,数据如下
①根据质量守恒定律,反应中共生成二氧化碳质量为3.3g
②请列式计算每片此钙片含碳酸钙的质量.
③请计算每片此钙片的含钙量,并建议厂家如何修改标签.
药品:氯酸钾、高锰酸钾、大理石、二氧化锰、稀盐酸、过氧化氢溶液.
仪器:图1

(1)请从图1仪器中选择适当的仪器组装一套实验室制取二氧化碳的装置(包括发生装置和收集装置):ABGD,写出反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)如果选用碳酸钠粉末和稀盐酸来制取二氧化碳,为了控制反应速率,应对该气体发生装置如何改进?(可另增仪器)分液漏斗.
(3)利用(1)中装置和以上药品还可以制取氢气,选择的药品是:锌粒和稀硫酸.
(4)某钙片的标签如图2,且知钙片中只有碳酸钙中含有钙元素,但人们发现其中的含钙量是不符合事实的;某实验小组为测定其真实的含钙量做了如下实验,每次取10片钙片放入已称量的含足量盐酸的烧杯中,充分反应后称取烧杯和剩余物质的总质量,数据如下
| 物质的质量 | |
| 反应前:烧杯+盐酸 | 50g |
| 10片钙片 | 10g |
| 反应后:烧杯+剩余物 | 56.7g |
②请列式计算每片此钙片含碳酸钙的质量.
③请计算每片此钙片的含钙量,并建议厂家如何修改标签.
19.下列过程中发生化学变化的是( )
| A. | 海水晒盐 | B. | 干冰制冷 | C. | 铁矿石炼铁 | D. | 风能发电 |
16.如图实验不能达到目的是( )
| A. |  验证CO2密度大于空气 | B. |  验证不同物质的着火点不同 | ||
| C. |  验证质量守恒定律 | D. |  探究金属和合金的硬度 |
3.下列说法不正确的是( )
| A. | 用红磷测定空气中氧气含量时,红磷一定要过量 | |
| B. | 实验室用过氧化氢制氧气的反应中,二氧化锰起催化作用 | |
| C. | 硫粉在氧气中燃烧时,集气瓶中放少量水可吸收二氧化硫 | |
| D. | 用排水法收集氧气时,导管口刚有气泡冒出就收集气体 |
20.如表实验操作、现象与结论对应关系正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用黄铜片在铜片上刻画 | 铜片上有划痕 | 黄铜的硬度比铜大 |
| B | 将两根铁丝分别伸到CuSO4溶液和AgNO3溶液中 | 两根铁丝表面均有固体附着 | 金属的活动性是Fe>Cu>Ag |
| C | 向某溶液中滴入无色酚酞试液 | 无色酚酞试液不变色 | 无色溶液一定是酸 |
| D | 向某物质加入稀硫酸 | 有气泡产生 | 该物质一定含CO32- |
| A. | A | B. | B | C. | C | D. | D |
17.某化学反应为:H2S+Cl2═2HCl+S↓ 该反应的类型为( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |