题目内容
13.框图中的物质均为初中化学常见的物质,其中A是建筑材料的主要成分,B属于氧化物,如图是它们之间的相互转化关系.请回答: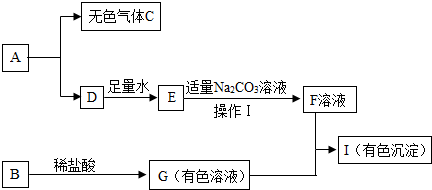
(1)写出下列物质的化学式:A、CaCO3,C、CO2.
(2)得到F溶液的操作Ⅰ的名称为:过滤.
(3)若I是红褐色沉淀,请写出G+F→I的化学方程式:2NaOH+CuCl2=Cu(OH)2↓+2NaCl;若I是蓝色沉淀,其化学式为Cu(OH)2.
(4)指出反应A-D+C的基本类型是分解反应.
分析 根据图中的物质均为初中常见的物质,A是建筑材料的主要成分,所以A是碳酸钙,碳酸钙在高温的条件下分解会生成二氧化碳和氧化钙,所以C是二氧化碳,D就是氧化钙,氧化钙和水反应会生成氢氧化钙,所以E是氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以F是氢氧化钠,氧化物B和盐酸反应会生成蓝色的溶液,所以B是氧化铜,G就是氯化铜,氢氧化钠和氯化铜反应会生成有色的沉淀,所以I是氢氧化铜,然后将推出的各种物质代入转化关系中验证即可.
解答 解:(1)图中的物质均为初中常见的物质,A是建筑材料的主要成分,所以A是碳酸钙,碳酸钙在高温的条件下分解会生成二氧化碳和氧化钙,所以C是二氧化碳,D就是氧化钙,氧化钙和水反应会生成氢氧化钙,所以E是氢氧化钙,氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,所以F是氢氧化钠,氧化物B和盐酸反应会生成蓝色的溶液,所以B是氧化铜,G就是氯化铜,氢氧化钠和氯化铜反应会生成有色的沉淀,所以I是氢氧化铜,推出的各种物质代入转化关系中经过验证均满足题意,推导合理,A是CaCO3,C是CO2;
(2)过滤的方法可以将不溶物和可溶物进行分离,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,要除去碳酸钙沉淀得到氢氧化钠溶液,可以使用过滤的方法;
(3)G是氯化铜,F是氢氧化钠,氢氧化钠能氯化铜反应生成氢氧化铜沉淀和氯化钠,化学方程式为:2NaOH+CuCl2=Cu(OH)2↓+2NaCl;
(4)A-D+C是碳酸钙高温分解生成二氧化碳和氧化钙,属于分解反应;
故答案为:(1)CaCO3,CO2;
(2)过滤;
(3)2NaOH+CuCl2=Cu(OH)2↓+2NaCl;Cu(OH)2;
(4)分解.
点评 本题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用物质的性质进行顺向或逆向或两边向中间推,逐一导出其他结论,最后带入验证.

 名校课堂系列答案
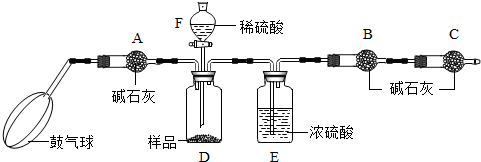
名校课堂系列答案 老师向同学们展示了一瓶标签受损的无色溶液(如图所示),并要求同学们进行探究.
老师向同学们展示了一瓶标签受损的无色溶液(如图所示),并要求同学们进行探究.【提出问题】这瓶无色溶液是什么溶液?
【提出猜想】老师提示:这瓶无色溶液可能是下列四种溶液中的一种:
①MgSO4 ②Na2SO4 ③H2SO4 ④BaSO4
【查阅资料】:Na2SO4的水溶液显中性.
【实验探究】
(1)依据溶解度性,猜想中一定不成立的是④(填序号);
(2)为确定其它几种猜想是否正确,小明同学进行如表探究:
| 实验操作 | 实验现象 | 实验结论 |
| 第一步:取待测溶液少许于试管甲中,向其中滴加几滴NaOH溶液 | 产生白色沉淀 | 猜想①成立 |
| 第二步:另取待测溶液少许于试管乙中,向其中滴加无色酚酞试液 | 无明显现象 | 猜想③成立 |
(3)请你设计实验方案,确认该溶液是H2SO4溶液,并完成如表实验报告:
| 实验操作 | 实验现象 | 实验结论 |
| 取该少许于试管丙中,加入铁粉 | 有气泡产生 | 猜想③成立,该反应的化学方程式为Fe+H2SO4═FeSO4+H2↑ |
| A. | CaO | B. | CO2 | C. | CaCO3 | D. | Na2SO4 |
| KCl溶液 | Na2CO3溶液 | Ba(NO3)2溶液 | |
| 物质X | 无明显现象 | 产生气体 | 产生白色沉淀 |
| A. | 澄清石灰水 | B. | 稀盐酸 | C. | 稀硫酸 | D. | 酚酞试液 |
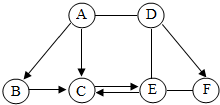 如图 A、B、C、D、E、F为初中化学常见的六种含氧化合物,A、B、C 均由两种元素组成,在常温下状态各不相同,其中A为红色粉末,D、E、F 均由三种元素组成,且物质类别各不相同.“→”表示物质间的转化关系,“-”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).回答下列问题:
如图 A、B、C、D、E、F为初中化学常见的六种含氧化合物,A、B、C 均由两种元素组成,在常温下状态各不相同,其中A为红色粉末,D、E、F 均由三种元素组成,且物质类别各不相同.“→”表示物质间的转化关系,“-”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).回答下列问题:
 已知:“
已知:“ ”代表氢原子,“
”代表氢原子,“ ”代表碳原子,“
”代表碳原子,“ ”代表氧原子)
”代表氧原子)