题目内容
17.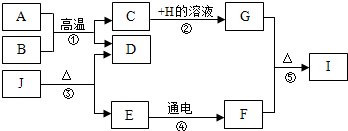 A~J分别为九年级化学学过的不同物质,它们存在如图所示的转化关系.已知A为铁锈的主要成分,E在常温下为液体,H的溶液呈蓝色,常温下B、D、F均为无色气体,其中J不稳定,受热易分解.(反应②、④的个别生成物已略去)
A~J分别为九年级化学学过的不同物质,它们存在如图所示的转化关系.已知A为铁锈的主要成分,E在常温下为液体,H的溶液呈蓝色,常温下B、D、F均为无色气体,其中J不稳定,受热易分解.(反应②、④的个别生成物已略去)(1)写出化学式:JH2CO3;FO2.
(2)写出反应①的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)写出反应⑤的化学方程式:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
分析 根据A~J分别为九年级化学学过的不同物质,根据“A为铁锈的主要成分”,所以A为氧化铁,B为气体,氧化铁和B反应后又生成了气体D,所以可以判断B为一氧化碳,而D为二氧化碳,那么C就是铁,根据“H为蓝色溶液”,可以知道H为铜盐的溶液,那么生成G应该为铜或是亚铁盐,根据“E在常温下为液体”,E在通电的条件下反应生成F,而F能和G反应,所以可以判断E为水,F为氧气,而G应该为铜单质,所以I为氧化铜,根据“常温下B、D、F均为无色气体,其中J不稳定,受热易分解”,J分解生成二氧化碳、水,所以可以判断J可能为碳酸,然后将推出的各种物质代入转化关系中验证即可.
解答 解:(1)根据A~J分别为九年级化学学过的不同物质,根据“A为铁锈的主要成分”,所以A为氧化铁,B为气体,氧化铁和B反应后又生成了气体D,所以可以判断B为一氧化碳,而D为二氧化碳,那么C就是铁,根据“H为蓝色溶液”,可以知道H为铜盐的溶液,那么生成G应该为铜或是亚铁盐,根据“E在常温下为液体”,E在通电的条件下反应生成F,而F能和G反应,所以可以判断E为水,F为氧气,而G应该为铜单质,所以I为氧化铜,根据“常温下B、D、F均为无色气体,其中J不稳定,受热易分解”,J分解生成二氧化碳、水,所以可以判断J可能为碳酸,然后将推出的各种物质代入转化关系中验证,推导正确,所以J为H2CO3;F为O2;
(2)反应①是一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,
反应④是铜与氧气生成氧化铜,化学方程式为:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
故答案为:
(1)H2CO3;O2;(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.(3)2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

| A. | 用过氧化氢制取氧气实验中,可以用氧化铜粉末、硫酸铜溶液或红砖粉末替代二氧化锰作催化剂 | |
| B. | 用明矾净化水的实验中,可以用硫酸铝替代明矾作絮凝剂 | |
| C. | 实验装置的组装顺序要遵循“从左到右、从上到下”的原则,拆卸装置刚好相反 | |
| D. | 蒸发食盐溶液时发现液滴飞溅,应立即停止加热,利用余热将溶液蒸干 |
| 选项 | 操作或现象 | 分子的特性 |
| ① | 25m3的石油气在加压装入容积为0.024m3的钢瓶中 | 分子间有间隔 |
| ② | 经过加油站常闻到汽油的气味 | 分子是运动的 |
| ③ | 100mL氧气和100mL氮气混合在一起,体积小于200mL | 分子的质量非常小 |
| ④ | 加热氧化汞可得到金属汞和氧气 | 分子是可以再分的 |
| A. | ① | B. | ② | C. | ③ | D. | ④ |
| A. | 通常雨水pH═5.6的原因:SO2+H2O═H2SO3 | |
| B. | 将鸡蛋放入盐酸中,蛋壳表面有气泡:CaCO3+2HCl═CaCl2+H2O+CO2↑ | |
| C. | 工业上用赤铁矿炼铁的主要反应:4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 | |
| D. | 成语:“滴水穿石”的反应:Ca(HCO3)2═CaCO3↓+CO2↑+H2O |
 如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在). 下列说法正确的是( )
如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在). 下列说法正确的是( )| A. | 三种物质溶解度大小依次为:乙>丙>甲 | |
| B. | 将温度由t2℃降到t1℃时,析出甲的质量比乙多 | |
| C. | 若甲中含有少量杂质乙,可采用降温结晶的方法进行提纯 | |
| D. | 将温度由t2℃降到t1℃,所得溶液中溶质的质量分数由大到小的顺序为:乙>丙=甲 |
| A. |  铁丝在氧气中燃烧 | B. |  检验CO2 | ||
| C. |  测溶液PH值 | D. |  过滤 |
 某研究性学习小组的同学按如图所示实验进行探究(其中A、B、C装置内的药品依次为石灰石和稀盐酸、紫色石蕊溶液、澄清石灰水),观察到烧杯内燃着的蜡烛从下而上依次熄灭,从这个实验中可以得出的那些探究结论?
某研究性学习小组的同学按如图所示实验进行探究(其中A、B、C装置内的药品依次为石灰石和稀盐酸、紫色石蕊溶液、澄清石灰水),观察到烧杯内燃着的蜡烛从下而上依次熄灭,从这个实验中可以得出的那些探究结论?