题目内容
下列图象与对应实验相符合的是
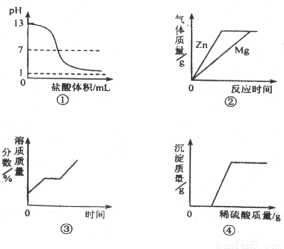
A.图①表示向pH=13的氢氧化钠溶液中逐滴加入pH=1的 盐酸
B.图②表示向溶质质量分数相同、等质量的稀硫酸中分别加入足量的金属镁和锌
C.图③表示将一定质量的不饱和硝酸钾溶液恒温蒸发至有晶体析出
D.图④表示向氢氧化钠与氯化钡的混合溶液中逐滴加入稀硫酸
A 【解析】 试题分析:A、pH=13的氢氧化钠溶液中逐滴加入pH=1的盐酸发生中和反应,生成中性物质,碱性不断减弱至恰好反应时PH=7,再滴加盐酸酸性会不断增强,但不可能达到PH=1,故此选项正确;B、镁与锌是镁的活动性较强一些,加入盐酸时应该是镁反应较快,而图象是体现锌的速度快一些,故此选项错误;C、一定质量的不饱和硝酸钾溶液恒温蒸发至有晶体析出的过程,是溶液由不饱和变成饱和的过程...
练习册系列答案
相关题目
一些常见物质的 pH 值如下,酸性最强的是( )
物质 | 牛奶 | 泡菜 | 肥皂 | 柠檬汁 |
物质 pH | 6.3 ~ 6.6 | 3.4 ~ 4.0 | 9.5 ~ 10.5 | 2.0 ~ 3.0 |
A. 牛奶 B. 泡菜 C. 肥皂 D. 柠檬汁
D 【解析】A、牛奶的pH为6.3 ~ 6.6,小于7,显酸性;B、泡菜的pH为3.4 ~ 4.0,小于7,显酸性;C、肥皂的pH为9.5 ~ 10.5,大于7,显碱性;D、柠檬汁的pH为2.0 ~ 3.0,小于7,显酸性。根据当溶液的pH小于7时,呈酸性,且pH越小,酸性越强,柠檬汁的pH最小,酸性最强。故选D。故选A。为探究盐酸的化学性质,某同学做了如下实验:
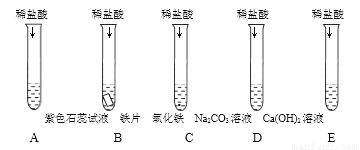
①A 中的现象是______;B 中反应的化学方程式为____;C 中反应原理的用途____;
②反应结束后,将 D、E 中的废液倒入同一个洁净的烧杯中,观察到先有气泡产生,后有白 色沉淀生成。过滤,得到白色沉淀和无色滤液。该同学欲探究无色滤液中的溶质。
无色滤液中一定不含 HCl,理由______(用化学方程式解释)。
【提出问题】无色滤液中的溶质是什么?
【作出猜想】①NaCl;②NaCl和CaCl2;③NaCl和Na2CO3;④NaCl、CaCl2和Na2CO3。 你认为猜想______一定不正确?
【进行实验】
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加少量碳酸钠溶液 | 无明显现象 | 猜想______成立 |
取少量滤液于试管中,滴加少量___ | 有气泡产生 |