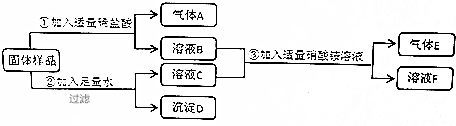
题目内容
13.将6g生铁放入盛有196g的5%硫酸溶液的烧杯中充分反应,若它们恰好反应,求:(1)反应生成氢气质量是多少?
(2)生铁中铁的质量分数.
分析 铁与稀硫酸反应生成硫酸亚铁和氢气,由参加反应的硫酸溶液的质量、溶质的质量分数,由反应的化学方程式,列式计算出生成氢气的质量、参加反应的铁的质量,进而计算出生铁中铁的质量分数.
解答 解:196g的5%硫酸溶液中含硫酸的质量为196g×5%=9.8g.
设生成氢气的质量为x,参加反应的铁的质量为y
Fe+H2SO4═FeSO4+H2↑
56 98 2
y 9.8g x
(1)$\frac{98}{2}=\frac{9.8g}{x}$ x=0.2g
(2)$\frac{56}{98}=\frac{y}{9.8g}$ y=5.6g
生铁中铁的质量分数为$\frac{5.6g}{6g}$×100%≈93.3%.
答:(1)反应生成氢气质量是0.2g
(2)生铁中铁的质量分数为93.3%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
3.下列对一些事实的解释不正确的是( )
| 事实 | 解释 | |
| A | 用碳素墨水书写档案 | 常温下单质碳的化学性质稳定 |
| B | 石墨能够做电池的电极材料 | 石墨较软 |
| C | 焦炭可以把铁从它的氧化物矿石里还原出来 | 焦炭具有还原性 |
| D | 制糖工业中用活性炭来脱色以制白糖 | 活性炭具有吸附性 |
| A. | A | B. | B | C. | C | D. | D |
4.下列除去杂质的方法错误的是(括号内的物质为杂质)( )
| A. | CO2(CO):通过的灼热的氧化铜 | B. | N2(O2):通过灼热铜网 | ||
| C. | CaCl2(CaCO3):溶解、过滤、蒸发 | D. | H2(CO2):通过浓氢氧化钠溶液 |
8.下列元素属于人体所需微量元素的是( )
| A. | 锌 | B. | 氧 | C. | 钙 | D. | 氢 |
5.下列方法不能达到实验目的是( )
| A. | 用水区分烧碱和硝酸铵两种固体 | |
| B. | 用硝酸银溶液区分氯化钠和氯化钙溶液 | |
| C. | 除去氧化铜中含有的铜粉:在空气中加热 | |
| D. | 除去二氧化碳中含有的水蒸气,将气体通过浓硫酸 |
16.下列化学符号与含义相符的是( )
| A. | Fe2+:1个铁离子 | B. | 3O:3个氧分子 | ||
| C. | 2OH-:2个氢氧根离子 | D. | N2:2个氮原子 |