题目内容
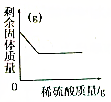
18.图1是实验室常用的实验装置.请回答下列问题:
(1)写出仪器a的名称:锥形瓶
(2)实验室用高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.若用C装置收集一瓶较纯净氧气,当观察到导管口有连续均匀气泡冒出时才可以收集.

(3)小明利用T形三通管(如图3)设计了探究二氧化碳性质的实验.在通入氧化碳气体后,观察到的实验现象是干燥的石蕊纱布不变色,湿润的石蕊纱布变红色,有关化学方程式是CO2+H2O=H2CO3
(4)已知H2S气体是一种有毒气体,溶于水会生成氢硫酸.某同学用图2装置来收集并处理多余的气体H2S.
①用该装置来收集处理H2S气体,证明H2S气体的密度比空气大.
②该装置中氢氧化钠溶液的作用是吸收硫化氢气体,防止空气污染.
分析 锥形瓶是常用的反应容器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.用排水法收集较纯净氧气的适宜时间是:当导管口有连续均匀气泡冒出时.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.图3中的现象是:干燥的石蕊纱布不变色,湿润的石蕊纱布变红色,因为二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液变红色;用图2装置来收集并处理多余的气体H2S,说明H2S气体的密度比空气大,该装置中氢氧化钠溶液的作用是:吸收硫化氢气体,防止空气污染.
解答 解:(1)锥形瓶是常用的反应容器,故答案为:锥形瓶;
(2)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;用排水法收集较纯净氧气的适宜时间是:当导管口有连续均匀气泡冒出时;故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;导管口有连续均匀气泡冒出;
(3)图3中的现象是:干燥的石蕊纱布不变色,湿润的石蕊纱布变红色,因为二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液变红色;故答案为:干燥的石蕊纱布不变色,湿润的石蕊纱布变红色;CO2+H2O=H2CO3;
(4)用图2装置来收集并处理多余的气体H2S,说明H2S气体的密度比空气大,该装置中氢氧化钠溶液的作用是:吸收硫化氢气体,防止空气污染;故答案为:大;吸收硫化氢气体,防止空气污染;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的性质和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 纯碱 NaOH | B. | 酒精 C2H5OH | C. | 生石灰 Ca(OH)2 | D. | 小苏打 Na2CO3 |
| A. | 用肥皂水鉴别软水和硬水 | |
| B. | 用带火星的木条鉴别空气和氧气 | |
| C. | 用稀HCl除去Na2SO4溶液中少量的Na2CO3 | |
| D. | 用溶解,过滤的方法除去MnO2粉末中少量的KCl固体 |
 课外活动中,化学兴趣小组的同学们进行了以下实验.为了验证质量守恒定律,同学们设计了如图所示的实验装置,其中气球的作用是:缓冲作用;镁粉燃烧的现象是产生耀眼的白光,放热,生成白色粉末;请从微观的角度解释燃烧前后质量守恒的原因化学反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化.
课外活动中,化学兴趣小组的同学们进行了以下实验.为了验证质量守恒定律,同学们设计了如图所示的实验装置,其中气球的作用是:缓冲作用;镁粉燃烧的现象是产生耀眼的白光,放热,生成白色粉末;请从微观的角度解释燃烧前后质量守恒的原因化学反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化.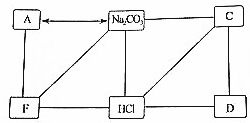 图是六种物质之间的转化关系.用“-”表示两种物质之间能发生反应,用“→”表示一种物质可以转化成另一种物质.A,B,C,D,E,F六种物质中,B,E已给出,其他四种物质分别为碱,盐,氧化物和黑色的金属粉末中的一种,回答下列问题:
图是六种物质之间的转化关系.用“-”表示两种物质之间能发生反应,用“→”表示一种物质可以转化成另一种物质.A,B,C,D,E,F六种物质中,B,E已给出,其他四种物质分别为碱,盐,氧化物和黑色的金属粉末中的一种,回答下列问题: