题目内容
20.下列物质分类的正确组合是( )| 碱 | 酸 | 盐 | 非金属氧化物 | |
| A | 纯碱 | HNO3 | 胆矾 | SO2 |
| B | 烧碱 | H2SO4 | NaCl | CO |
| C | 苛性钠 | HCl | 石灰石 | NO2 |
| D | 熟石灰 | H2CO3 | 苏打 | MnO2 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据常见物质的组成特点分析物质的类别.
解答 解:A、纯碱是碳酸钠属于盐,不属于碱,HNO3属于酸,胆矾属于盐,SO2属于非金属氧化物,故A错误;
B、烧碱是氢氧化钠属于碱,H2SO4属于酸,NaCl属于盐,CO属于非金属氧化物,故B正确;
C、苛性钠是氢氧化钠属于碱,HCl属于酸,石灰石主要成份是碳酸钙还含有杂质,属于混合物,NO2属于非金属氧化物,故C错误
D、熟石灰属于碱,H2CO3属于酸,苏打是碳酸钠属于盐,MnO2属于金属氧化物,故D错误.
故选B.
点评 了解酸、碱、盐等概念的定义和常见物质的组成特点、俗名等知识是解答本题基础.

练习册系列答案
相关题目
10.下列关于水的一些性质的描述中,属于化学性质的是( )
| A. | 水在4℃时的密度为1g/cm3 | B. | 在降低温度的情况下,水能结成冰 | ||
| C. | 水在101KPa时的沸点为100℃ | D. | 水在通电条件下能分解 |
8.水的净化方法有很多,下列方法中净化程度最高的是( )
| A. | 蒸馏 | B. | 吸附 | C. | 沉淀 | D. | 过滤 |
17.下列实验操作正确的是( )
| A. |  气体验满 | B. |  量取8.5mL液体 | C. |  给液体加热 | D. |  称量NaCI |
18.周期表中元素的结构和性质呈现一定的规律性变化.下表列出的是第三周期元素的原子半径及主要化合价(部分信息未列出)
(1)关于上表有以下说法,其中不正确的是D(填字母)
A.⑤处的最高正价是+6,最低负价是-2
B.③处的数值介于1.10-1.43之间
C.第三周期元素(Na→Cl)的最高正价数等于其原子的最外层电子数
D.元素①的原子序数是13,①和②形成的化合物的化学式为AlS
(2)表中不同种元素最本质的区别是A(填序号).
A.质子数不同 B.相对原子质量不同 C.电子数不同
(3)已知氟元素与氯元素位于同一纵行,化学性质相似,其原因是最外层电子数相同,它们在化学反应中都易得到(填“得到”或“失去”)电子.
| 元素 | Na | Mg | ① | Si | P | ② | Cl |
| 原子的最外层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 原子半径(10-10m) | 1.86 | 1.60 | 1.43 | ③ | 1.10 | 1.02 | 0.994 |
| 最高正价 最低负价 | +1 | +2 | ④ | +4 -4 | +5 -3 | ⑤ | +7 -1 |
A.⑤处的最高正价是+6,最低负价是-2
B.③处的数值介于1.10-1.43之间
C.第三周期元素(Na→Cl)的最高正价数等于其原子的最外层电子数
D.元素①的原子序数是13,①和②形成的化合物的化学式为AlS
(2)表中不同种元素最本质的区别是A(填序号).
A.质子数不同 B.相对原子质量不同 C.电子数不同
(3)已知氟元素与氯元素位于同一纵行,化学性质相似,其原因是最外层电子数相同,它们在化学反应中都易得到(填“得到”或“失去”)电子.
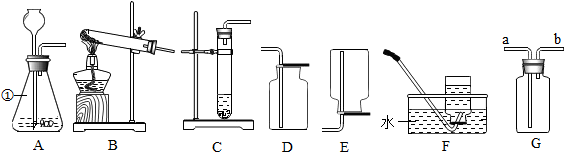
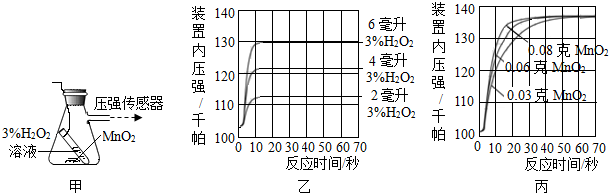
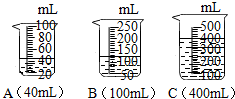
 某班同学在做测定红磷燃烧前后质量变化情况的实验,实验装置如图.
某班同学在做测定红磷燃烧前后质量变化情况的实验,实验装置如图.