题目内容
5.(1)四氧化三铁Fe3O4:相对分子质量232,各元素质量比21:8,各原子个数比3:4,铁元素的质量分数72.4%.(2)硫化亚铁FeS2:相对分子质量120,各元素质量比7:8,各原子个数比1:2,铁元素的质量分数46.7%.
分析 根据相对分子质量=相对原子质量与相应原子个数的乘积和;
元素质量比=相对原子质量与相应原子个数的乘积比;
根据分子是由原子构成的解答;
根据某元素质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%解答.
解答 解:(1)相对分子质量=相对原子质量与相应原子个数的乘积和,则四氧化三铁的相对分子质量=56×3+16×4=232;
元素质量比=相对原子质量与相应原子个数的乘积比,所以四氧化三铁中铁、氧两种元素的质量比=(56×3):(16×4)=168:64=21:8;
各原子个数比为:Fe:O=3:4;
四氧化三铁中铁的质量分数=$\frac{56×3}{232}$×100%≈72.4%;
(2)硫化亚铁FeS2的相对分子质量=56+32×2=120;
硫化亚铁FeS2中铁、硫两种元素的质量比=56:(32×2)=7:8;
各原子个数比=1:2;
硫化亚铁FeS2中铁的质量分数=$\frac{56}{120}×$100%≈46.7%.
答案:
(1)232;21:8;3:4;72.4%;
(2)120;7:8;1:2;46.7%.
点评 明确依据物质的化学式的相关计算方法,并能结合化学式正确分析解答.

练习册系列答案
相关题目
15.下列四种粒子的结构示意图中表示阴离子的是( )
| A. | 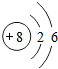 | B. | 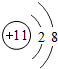 | C. | 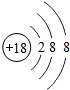 | D. | 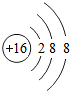 |
16.生活离不开化学.下列做法中,合理的是( )
| A. | 青少年适量补充微量元素铁以预防佝偻病 | |
| B. | 为了节约粮食,把霉变大米淘净后继续食用 | |
| C. | 利用硝酸铵溶于水吸热的原理,自制冰袋给发烧病人降温 | |
| D. | 食用甲醛浸泡的海产品,可提高人体免疫力 |
2.下列反应中,属于氧化反应,但不属于化合反应或分解反应的是( )
| A. | 石蜡+氧气$\stackrel{点燃}{→}$二氧化碳+水 | B. | 氧化汞$\stackrel{加热}{→}$汞+氧气 | ||
| C. | 硫+氧气$\stackrel{点燃}{→}$二氧化硫 | D. | 石灰石+盐酸→氯化钙+二氧化碳+水 |
3.下列实验现象描述正确的是( )
| A. | 白磷燃烧产生大量的白雾 | B. | 点燃纯净氢气产生淡蓝色火焰 | ||
| C. | 铁丝在空气中燃烧火星四射 | D. | 硫在空气中燃烧产生蓝紫色火焰 |