题目内容
15.在盛有100g稀盐酸的烧杯中放入10g碳酸钙粉末,一段时间后恰好完全反应.求:(1)生成二氧化碳气体的质量.
(2)稀盐酸的质量分数;
(3)生成物溶液中溶质的质量分数.
分析 碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳;由参加反应的碳酸钙的质量,列式计算出生成二氧化碳的质量、参加反应的盐酸的质量、生成氯化钙的质量,进而计算出稀盐酸的质量分数、生成物溶液中溶质的质量分数即可.
解答 解:设生成二氧化碳的质量为x,参加反应的盐酸的质量为y,生成氯化钙的质量为z,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 111 44
10g y z x
(1)$\frac{100}{44}=\frac{10g}{x}$ x=4.4g
(2)$\frac{100}{73}=\frac{10g}{y}$ y=7.3g
稀盐酸的质量分数为$\frac{7.3g}{100g}×$100%=7.3%.
(3)$\frac{100}{111}=\frac{10g}{z}$ z=11.1g
生成物溶液中溶质的质量分数为$\frac{11.1g}{10g+100g-4.4g}×$100%≈10.5%.
答:(1)生成二氧化碳气体的质量为4.4g;(2)稀盐酸的质量分数为7.3%;(3)生成物溶液中溶质的质量分数为10.5%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
6.豆浆被称为“植物奶”,其中含有异黄酮(C15H10O2)具有防癌功能,下列关于异黄酮说法正确的是( )
| A. | 异黄酮是由15个碳原子、10个氢原子、2个氧原子构成 | |
| B. | 异黄酮中碳元素质量分数最大 | |
| C. | 异黄酮的相对分子量为222g | |
| D. | 异黄酮中碳、氢、氧元素质量比为15:10:2 |
3.在天平左、右两盘中各放一个等质量的烧杯,烧杯中分别盛等质量的足量的稀硫酸,天平平衡.向左盘烧杯中加入65g锌粒,向右盘烧杯中加入氧化铜粉末,若天平最终平衡,则加入氧化铜粉末的质量为( )
| A. | 65g | B. | 63g | C. | 62 g | D. | 50g |
7.下列说法正确的是( )
| A. | NaNO2是一种氧化物 | |
| B. | NaNO2是由三种元素组成 | |
| C. | NaNO2中氮元素的化合价为-3价 | |
| D. | NaNO2中Na、N、O三种元素的质量比为1:1:2 |
13.如图所示的实验操作不正确的是( )
| A. | 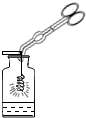 铁丝在氧气中燃烧 | B. |  读取液体的体积 | ||
| C. | 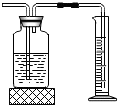 测定高锰酸钾分解生成氧气的体积 | D. | 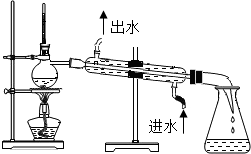 制取蒸馏水 |

