题目内容
13.室温下,分别向四个装有等质量的水的烧杯中加入硝酸钾固体,且所加固体的质量依次减少,充分溶解后如图所示,请回答下列问题.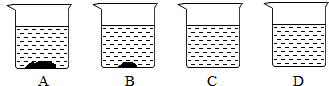
(1)AB中盛的一定是饱和溶液;C中盛的可能是饱和溶液,D中盛的一定是不饱和溶液(以上均填序号);
(2)若对A、B两烧杯进行加热,随着温度的升高,先变成不饱和溶液的是B(填序号);
(3)欲使接近饱和的硝酸钾溶液变为饱和溶液,可采取的方法是蒸发水分.(写出一种方法即可)
分析 (1)根据饱和溶液的判断方法考虑;根据固体溶质质量依次减少考虑;根据不饱和溶液的判断方法考虑;
(2)根据A、B烧杯中固体的多少进行分析;
(3)根据硝酸钾的溶解度随温度的升高而增大进行分析.
解答 解:(1)饱和溶液是在该温度下不能再溶解该物质的溶液,由图示可知A和B中都有固体溶质的不溶物,所以都为饱和溶液;由于C中没有固体溶质不溶物,有两种可能:有可能刚好饱和,也有可能不饱和,所以C中盛的可能是饱和溶液;D中也没有固体溶质不溶物,按常规考虑有两种可能:有可能刚好饱和,也有可能不饱和,因为固体溶质质量依次减少,C中可能饱和或不饱和,D中溶质比C中少,所以D溶液一定不饱和;
(2)B烧杯中的固体比A烧杯中的少,所以若对A、B两烧杯进行加热,随着温度的升高,先变成不饱和溶液的是B;
(3)硝酸钾的溶解度随温度的升高而增大,所以欲使接近饱和的硝酸钾溶液变为饱和溶液,可采取的方法是蒸发水分.
故答案为:(1)A、B,C,D;
(2)B;
(3)蒸发水分(或降低温度).
点评 解答本题关键是要知道饱和溶液和不饱和溶液的判断,有固体不溶物的溶液,一定是这种物质的饱和溶液.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
3.石灰石是我国的主要矿产之一,为测定其中碳酸钙的含量,课外活动小组的同学称取50g石灰样品.分别在5只烧杯中进行了实验,实验数据见下表(假设每个烧杯中都充分反应,石灰石中其它成分既不溶于水,也不与水反应):
(1)表中X的值为37.36g;
(2)烧杯①②③(填序号)中反应后碳酸钙有剩余;
(3)烧杯④(填序号)中石灰石与稀盐酸恰好完全反应;
(4)求样品中碳酸钙的质量分数(写出计算过程)
| 烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
| 加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
| 加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
| 烧杯中剩余物质的质量/g | 19.12 | 28.24 | x | 46.48 | 56.48 |
(2)烧杯①②③(填序号)中反应后碳酸钙有剩余;
(3)烧杯④(填序号)中石灰石与稀盐酸恰好完全反应;
(4)求样品中碳酸钙的质量分数(写出计算过程)
8.用双氧水、氯酸钾和高锰酸钾等物质都能制得氧气,说明这些物质的组成中都含有( )
| A. | 氧气 | B. | 氧元素 | C. | 氧分子 | D. | 氧原子 |
5.过氧乙酸的化学式为C2H4O3.下列对过氧乙酸的说法不正确的是( )
| A. | 过氧乙酸是氧化物 | |
| B. | 它由碳、氢、氧三种元素组成 | |
| C. | 一个过氧乙酸分子中含有9个原子 | |
| D. | 其中碳、氢、氧的原子个数比为2:4:3 |
2.如图所示,某兴趣小组在进行酸碱中和反应的实验探究时,向氢氧化钠溶液中滴加稀盐酸,反应一段时间后,发现忘记滴加指示剂.甲同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.
(1)请写出上述反应的化学方程式:HCl+NaOH═NaCl+H2O.
【猜想与假设】
猜想一:两种物质已恰好完全中和,溶液呈中性;
猜想二:反应后氢氧化钠过量,溶液呈碱性;
猜想三:反应后盐酸过量,溶液呈酸性.
甲、丙两位同学经过讨论后认为猜想二不正确,原因是:酚酞试液在碱性溶液中为红色.
【设计并进行实验】
(2)为了验证猜想一,甲同学设计了如下实验方案:
(3)请你设计另一个实验(与甲同学方案不同)方案,验证猜想三,并填写下表:
(1)请写出上述反应的化学方程式:HCl+NaOH═NaCl+H2O.
【猜想与假设】
猜想一:两种物质已恰好完全中和,溶液呈中性;
猜想二:反应后氢氧化钠过量,溶液呈碱性;
猜想三:反应后盐酸过量,溶液呈酸性.
甲、丙两位同学经过讨论后认为猜想二不正确,原因是:酚酞试液在碱性溶液中为红色.
【设计并进行实验】
(2)为了验证猜想一,甲同学设计了如下实验方案:
| 实验步骤 | 实验现象 | 实验结论 |
| 用洁净干燥的玻璃棒蘸取少量反应后的溶液滴在干燥的pH试纸上,观察颜色变化并与标准比色卡对比. | pH<(填“>”、“=”或“<”)7 | 猜想一不成立 |
| 实验步骤 | 实验现象 | 实验结论 |
| 从烧杯中取少量反应后的溶液,滴入紫色石蕊试液 | 溶液变红 | 猜想三成立 |
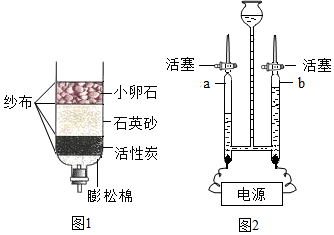 最近,据权威实验结果显示,我国的地表水被检测出含有68种抗生素,大部分地区水中检出的抗生素频率高达100%,水资源的安全问题再次引发民众的担忧,水和空气一样决定着我们的健康,而家用净水器在不少家庭中已成为不可缺少的滤水装置.
最近,据权威实验结果显示,我国的地表水被检测出含有68种抗生素,大部分地区水中检出的抗生素频率高达100%,水资源的安全问题再次引发民众的担忧,水和空气一样决定着我们的健康,而家用净水器在不少家庭中已成为不可缺少的滤水装置.
