题目内容
4. 最近,据权威实验结果显示,我国的地表水被检测出含有68种抗生素,大部分地区水中检出的抗生素频率高达100%,水资源的安全问题再次引发民众的担忧,水和空气一样决定着我们的健康,而家用净水器在不少家庭中已成为不可缺少的滤水装置.
最近,据权威实验结果显示,我国的地表水被检测出含有68种抗生素,大部分地区水中检出的抗生素频率高达100%,水资源的安全问题再次引发民众的担忧,水和空气一样决定着我们的健康,而家用净水器在不少家庭中已成为不可缺少的滤水装置.(1)提倡节约用水,保护水资源.列举日常生活中节约用水的两种方法:①淘米水浇花;②随手关闭水龙头.
(2)活性炭家用净水器是现在使用比较多的净水器,过滤后的自来水,无异味,改善了饮用水的水质.在水的净化过程中,利用了活性炭的吸附性去除某些杂质.
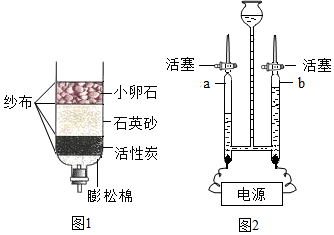
(3)明明同学自制了净化水的简易装置如图1所示,由此得到的水属于混合物(填“纯净物”或“混合物”).天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是蒸馏.明明同学可以用肥皂水检验所得自来水是否为硬水.
(4)条件不同,水可能发生不同的变化.如图2所示,通电一段时间后,试管a中所收集的气体为氢气,如何检验该气体:用燃着的木条检验氢气,现象是气体燃烧,有淡蓝色火焰,证明气体是氢气.试管a和试管b收集的气体体积比为2:1.该实验说明水是由氢元素和氧元素组成的.
(5)将电解水制得的4g氢气在氯气中燃烧,生成的氯化氢气体完全溶于1000L水中,计算得到的盐酸(HCl)中溶质的质量分数(水的密度是1g/mL,小数点后保留一位).
分析 (1)利用生活常识对经验,提出日常生活中可节约用水的做法;
(2)根据活性炭的吸附性来分析;
(3)根据水中还含有杂质、净化水的原理以及硬水的检验方法来分析;
(4)根据电解水产生的氢气体积大,氧气体积小,正极产生氧气,负极产生氢气,电解水获得的实验结论,要记住;
(5)根据化学方程式中氢气的质量可求生成的氯化氢质量;根据溶质质量分数公式计算.
解答 解:(1)节约用水的例子有许多,如一水多用:用淘米水浇花,用洗衣服的水冲厕所等;用完水后及时关闭水龙头,使用节水龙头,工业上污水经处理后再循环使用、农业上改变灌溉的方式、生活中加强节约用水的意识;故填:淘米水浇花;随手关闭水龙头;
(2)活性炭具有吸附性,能够吸附水中的色素和异味;故填:吸附;
(3)经此装置净化的水中还含有可溶性杂质,属于混合物;蒸馏获得的水是纯净水,是净化程度最高的净水方法;鉴别硬水和软水使用肥皂水,与肥皂水混合产生浮渣的是硬水,与肥皂水混合产生泡沫的是软水;降低水的硬度就是减少水中可溶性钙镁化合物的含量,可以采用加热煮沸或蒸馏的方法,故填:混合物;蒸馏;肥皂水;
(4)a管内的气体体积较大,是氢气,氢气具有可燃性,可用燃着的木条进行检验,b管内的气体体积较小,是氧气,氢气与氧气的体积比为2:1,电解水时产生了氢气和氧气,说明水是由氢元素和氧元素组成的.故填:氢气;用燃着的木条检验氢气,现象是气体燃烧,有淡蓝色火焰,证明气体是氢气;2:1;氢元素和氧元素
(5)解:设生成的氯化氢的质量为x.
H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl
2 73
4g x
$\frac{2}{73}=\frac{4g}{x}$
解得x=146g
盐酸中氯化氢的质量分数=$\frac{146g}{146g+1000mL×1g/mL}$≈12.7%
到的盐酸(HCl)中溶质的质量分数为12.7%
点评 本题考查了水的净化、水的电解以及有关物质间反应化学方程式的计算,完成此题,可以依据已有的知识进行.

| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | CO2气体 | CO气体 | 通入氧气,点燃 |
| B | CO气体 | CO2气体 | 通入足量氢氧化钠溶液 |
| C | CuO粉 | C粉 | 将混合物放在氧气流中灼烧 |
| D | KCl固体 | KClO3 | 加热混合物足量时间 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 对苯二胺中氮元素的质量分数是25% | |
| B. | 对苯二胺是由6个碳原子、8个氢原子和1个氮分子构成 | |
| C. | 对苯二胺中碳、氢、氮元素的质量比为3:4:1 | |
| D. | 对苯二胺的相对分子质量是108 |

| A. | 该反应属于置换反应 | B. | 反应中有三种氧化物 | ||
| C. | b,d两种物质均由分子构成 | D. | a物质中氮元素的化合价为+3价 |