题目内容
18.金属活动性顺序在工农业生产和科学研究中有重要应用.(1)铝比较活泼,为什么铝制品却有很好的抗腐蚀性能?
(2)为何农业上不能用铁桶配制波尔多液(含硫酸铜),请用化学方程式解释.
(3)如何判断Cu和Ag两种金属的活动性强弱?请写出实验方法,及可能的化学方程式.
分析 (1)根据铝与氧气反应生成物的特性分析回答;
(2)根据铁与硫酸铜的反应分析回答;
(3)在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,利用此知识分析即可.
解答 解:(1)由于铝易与氧气反应,生成致密的氧化铝薄膜,阻止铝进一步被氧化铝比较活泼,这是铝制品有很好的抗腐蚀性能的原因;
(2)由于铁比铜活泼,能将铜从其盐溶液中置换出来,所以不能用铁桶配制波尔多液(含硫酸铜),化学方程式为:Fe+CuSO4═FeSO4+Cu.
(3)常用金属与盐溶液能否反应来判断金属的活动性,要判断Cu和Ag两种金属的活动性强弱,可将铜丝放入硝酸银溶液中,铜丝表面有银白色物质析出,说明铜的活动性比银强;方程式:Cu+2AgNO3═Cu (NO3)2+2Ag.
故答为:(1)铝易与氧气反应,生成致密的氧化铝薄膜,阻止铝进一步被氧化.(2)Fe+CuSO4═FeSO4+Cu;(3)将铜丝放入硝酸银溶液中,铜丝表面有银白色物质析出,说明铜的活动性比银强;方程式:Cu+2 AgNO3═Cu(NO3)2+2Ag.
点评 本题考查了金属的性质以及活动性顺序表的应用,完成此题,可以依据金属活动性顺序的意义进行.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
20.某兴趣小组在进行实验室制取二氧化碳和性质的探究.
(1)选择药品.小明对三组药品进行了研究,实验记录如下:
从制取和收集的角度分析,一般选择第①组药品,该组药品发生反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;
不选择第③组药品的原因是反应速度太快不利于收集.
(2)选择装置.他选择图中B作为制取的发生装置.你认为他选择的依据是固体和液体发生反应,反应条件是常温,小丽认为利用B装置也可以选择第③组药品来制取二氧化碳,理由是利用分液漏斗控制液体流速,可以控制反应速度.

(3)制取气体.将药品装入所选装置制取气体,并只能用图中D组装置收集.原因是二氧化碳能溶于水,密度比空气大.
(4)气体检验.小明将生成的气体通入石蕊溶液中,溶液变红,因此他确定该气体是二氧化碳.他的检验方法是否正确?不正确请说明理由.因为还有其他气体也可以使紫色石蕊变红色.请写出正确的检验二氧化碳的方法:Ca(OH)2+CO2═CaCO3↓+H2O(用化学方程式表示).
(1)选择药品.小明对三组药品进行了研究,实验记录如下:
| 组别 | 药品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
不选择第③组药品的原因是反应速度太快不利于收集.
(2)选择装置.他选择图中B作为制取的发生装置.你认为他选择的依据是固体和液体发生反应,反应条件是常温,小丽认为利用B装置也可以选择第③组药品来制取二氧化碳,理由是利用分液漏斗控制液体流速,可以控制反应速度.

(3)制取气体.将药品装入所选装置制取气体,并只能用图中D组装置收集.原因是二氧化碳能溶于水,密度比空气大.
(4)气体检验.小明将生成的气体通入石蕊溶液中,溶液变红,因此他确定该气体是二氧化碳.他的检验方法是否正确?不正确请说明理由.因为还有其他气体也可以使紫色石蕊变红色.请写出正确的检验二氧化碳的方法:Ca(OH)2+CO2═CaCO3↓+H2O(用化学方程式表示).
13.下列实验操作正确的是( )
| A. | 熄灭酒精灯可用嘴吹灭 | |
| B. | 用高锰酸钾制氧气时,当水槽中出现气泡时立即收集 | |
| C. | 用剩的药品可放回原瓶 | |
| D. | 用高锰酸钾制氧气实验结束时,先从水槽中拿出导管后撤酒精灯 |

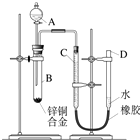 某学习小组用如右图所示装置测定锌铜合金中锌、铜的质量分数.
某学习小组用如右图所示装置测定锌铜合金中锌、铜的质量分数.