题目内容
8.为探究一瓶敞放的氢氧化钠固体的变质情况,同学们提出了下列猜想:A只有氢氧化钠固体
B只有碳酸钠固体
C你认为还可能是NaOH和Na2CO3的混合物固体
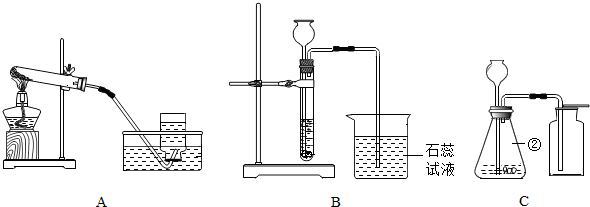
①取少量该固体样品置于试管中,向其中加入一种无色溶液,发现有气泡产生,说明该样品中含有碳酸钠,由此可确定该固体已发生变质.该固体变质的化学方程式2NaOH+CO2═Na2CO3+H2O;则无色溶液可能是稀盐酸或稀硫酸、稀硝酸.
②为探究该固体中是否还有未变质的氢氧化钠,同学们又进行了如下表所示的实验.已知碳酸钠的水溶液呈碱性,它的存在会对氢氧化钠的检验造成干扰.请根据下表部分物质的溶解性表(20℃)所提供的信息,将如表填写完整.
| 阴离子 阳离子 | OH- | NO3- | Cl- | SO42- | CO32- |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不溶 | 不溶 |
| 实验目的 | 实验操作 | 现象 | 结论或化学方程式 |
| 除去碳酸钠 | 取少量该固体样品溶于水配成溶液,滴加适量的BaCl2溶液.充分反应后过滤 | 有白色沉淀生成 | 有关反应的化学方程式为 Na2CO3+BaCl2═BaCO3↓+2NaCl |
| 检验是否含有氢氧化钠 | 在滤液中滴加酚酞溶液 | 变红 | 该样品中含有氢氧化钠 |
分析 根据氢氧化钠变质生成碳酸钠进行分析解答,检验变质就是检验碳酸钠的存在,检验变质的程度就是检验是否含有氢氧化钠,据此解答.
解答 解:氢氧化钠若是部分变质,则是氢氧化钠和碳酸钠的混合物,故填:NaOH和Na2CO3的混合物;
(1)氢氧化钠与二氧化碳反应生成碳酸钠而变质,碳酸钠能与酸反应产生气体,加入的无色液体就可以是稀盐酸、稀硫酸或是稀硝酸,故填:2NaOH+CO2═Na2CO3+H2O;稀盐酸或稀硫酸、稀硝酸;
(2)要检验氢氧化钠是否存在,可以加入氯化钡除去碳酸钠,然后加入酚酞试液,溶液变红,故填:BaCl2,Na2CO3+BaCl2═BaCO3↓+2NaCl;变红.
点评 本题考查的是氢氧化钠变质成分的实验探究,完成此题,可以依据已有知识进行.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
16.单质碘呈紫黑色晶体,易升华,有毒性和腐蚀性,碘单质遇淀粉水溶液会变蓝色,主要用于制药物、染料、碘酒、试纸和碘化合物等,碘是人体的必需微量元素之一.上述对碘的描述中,没有涉及到的是( )
| A. | 物理性质 | B. | 制法 | C. | 用途 | D. | 化学性质 |
17.下列说法正确的是( )
| A. | 棉、羊毛,塑料等都属于天然有机高分子材料 | |
| B. | 食用加碘食盐和强化铁酱油可补充某些人体必需微量元素 | |
| C. | 用甲醛水溶液浸泡水产品以防止腐烂 | |
| D. | 铁制品表面涂“银粉(铝粉)”防生绣,是由于铝的化学性质比铁稳定 |
18.浓盐酸敞口放置一段时间后,将会( )
| A. | 质量变小 | B. | 质量变大 | C. | 质量不变 | D. | 质量分数变大 |
 所示的粒子符号为Mg2+.
所示的粒子符号为Mg2+.