题目内容
2.请阅读下面短文,回答有关问题.人类创造肥皂的历史至少已有2300年了.早期的文明古国将肥皂用作染发剂或药物,直到公园100-199年,人们才逐渐认识到肥皂有去污作用,可用作清洗剂.起初人们利用草木灰(主要成分K2CO3)产生的碱液与油脂反应制造肥皂.大约到了1790年,法国科学家Nicolaos Leblanc发现碱可以用普通的食盐和水制得,这一发明使制皂变得更为容易.
肥皂溶液显碱性,它的主要成分是高级脂肪酸纳(如硬脂肪酸纳C17H35COONa),它是通过酸(如硬脂酸C17H35COOH)和碱反应而得到的产品.
肥皂有许多种类,如:加入Na2CO3等物质后的白色洗衣皂去污能力更强;在肥皂中加入硫磺即得到具有消炎、杀菌、控油作用的药皂-硫磺皂;香皂则是在肥皂中加入某些香料制成,其碱性较弱,对皮肤的刺激性较小.
(1)若用硬水洗衣服,当肥皂溶于水后产生的现象是泡沫少,浮渣多;
(2)硬脂酸中氢、氧元素的质量比是9:8;
(3)有皮肤病的人适宜使用的肥皂是硫磺皂;白色洗衣皂中与去污能能力增强有关的离子是CO32-.
分析 (1)根据硬水加入肥皂水会产生大量浮渣,无泡沫进行分析;
(2)根据元素质量比计算方法进行分析;
(3)根据硫磺皂的作用进行分析;根据白色洗衣皂中与去污能能力增强有关的离子进行分析.
解答 解:(1)在硬水中加入肥皂水,会形成大量浮渣,没有泡沫,衣物洗不干净;
故答案为:泡沫少,浮渣多;
(2)硬脂酸中氢、氧元素的质量比为(36×1):(2×16)=9:8.
故答案为:9:8;
(3)在肥皂中加入硫磺即得到具有消炎、杀菌、控油作用的药皂-硫磺皂;故有皮肤病的人适宜使用硫磺皂;白色洗衣皂中与去污能能力增强有关的离子是CO32-;
故答案为:硫磺皂;CO32-.
点评 本题考查化学与生活,体现了化学知识在生产、生活中的应用,注意知识的积累.

练习册系列答案
相关题目
11.下列图象能正确反映对应的反应过程的是( )
| A. |  将不饱和的硝酸钾溶液升温 | |
| B. |  向一定里的二氧化锰中加入过氧化氢溶液 | |
| C. |  向NaOH溶液中不断加水 | |
| D. |  向等质量的镁、锌中分別加入足量的稀硫酸 |
 水和溶液与人类生存和发展密切相关.
水和溶液与人类生存和发展密切相关.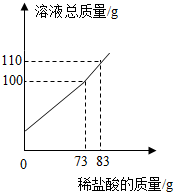 某纯碱样品中含少量氯化钠,称取11g样品于烧杯中,加20.4g的水将其全部溶解,再逐滴加入一定质量分数的稀盐酸并振荡,实验过程中,测得加入稀盐酸的质量和溶液总质量的关系如图所示,计算(写出计算过程):
某纯碱样品中含少量氯化钠,称取11g样品于烧杯中,加20.4g的水将其全部溶解,再逐滴加入一定质量分数的稀盐酸并振荡,实验过程中,测得加入稀盐酸的质量和溶液总质量的关系如图所示,计算(写出计算过程): .
.