题目内容
17.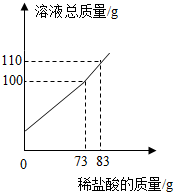 某纯碱样品中含少量氯化钠,称取11g样品于烧杯中,加20.4g的水将其全部溶解,再逐滴加入一定质量分数的稀盐酸并振荡,实验过程中,测得加入稀盐酸的质量和溶液总质量的关系如图所示,计算(写出计算过程):
某纯碱样品中含少量氯化钠,称取11g样品于烧杯中,加20.4g的水将其全部溶解,再逐滴加入一定质量分数的稀盐酸并振荡,实验过程中,测得加入稀盐酸的质量和溶液总质量的关系如图所示,计算(写出计算过程):(1)反应中生成二氧化碳的质量.
(2)样品中碳酸钠的质量分数.
分析 (1)根据质量守恒定律计算生成二氧化碳的质量;
(2)根据碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,依据二氧化碳的质量计算参加反应的碳酸钠的质量,然后计算质量分数.
解答 解:(1)根据质量守恒定律,反应后溶液减少的质量就是反应中生成的二氧化碳的质量为:11+73+20.4-100=4.4g;
(2)设参加反应的碳酸钠的质量是x
Na2C03+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{x}$=$\frac{44}{4.4g}$
x=10.6g
碳酸钠的质量分数为:$\frac{10.6g}{11g}$×100%=96.4%.
故答案为:(1)4.4g;
(2)碳酸钠的质量分数为96.4%.
点评 本题是对化学方程式计算的考查,解题的关键是找到已知量,此题则是利用反应前后物质质量的变化求出生成二氧化碳的质量,而后根据它的质量求出其它的需要的物质的质量解答即可.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
5. 学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液分别标记为甲、乙.请你和同学们一起完成探究过程:
学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液分别标记为甲、乙.请你和同学们一起完成探究过程:
【设计实验】
【科学探究】
(1)碳酸钠属于盐(选填“酸”、“碱”、“盐”)类物质,其水溶液显碱性.
(2)现象A是有气泡产生,则甲溶液是碳酸钠;产生该现象的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑;该反应属于基本反应类型中的复分解反应,步骤①乙溶液中溶质一定有氯化钙.
(3)根据步骤③实验现象则上层溶液中一定含有的溶质是氯化钠(酸碱指示剂除外),可能含有的溶质是氯化钙为验证可能含有的溶质,应该补充的实验操作是取样,滴加碳酸钠溶液.
【定量分析】
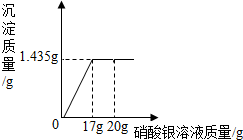
(4)已知酚酞与硝酸银不反应,同学们利用反应废液缸中的上层清液来测定某硝酸银溶液中溶质的质量分数.取上层清液,滴加硝酸银溶液,产生沉淀的质量变化如图所示,该硝酸银溶液溶质的质量分数为10%.
 学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液分别标记为甲、乙.请你和同学们一起完成探究过程:
学习完“酸、碱、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液分别标记为甲、乙.请你和同学们一起完成探究过程:【设计实验】
| 实验操作 | 实验现象 |
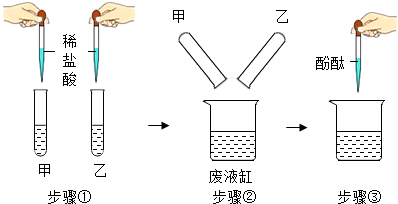 | 步骤①:甲溶液中观察到现象A, 乙溶液中无明显现象 步骤②:底部有白色沉淀 步骤③:上层为无色透明的溶液 |
(1)碳酸钠属于盐(选填“酸”、“碱”、“盐”)类物质,其水溶液显碱性.
(2)现象A是有气泡产生,则甲溶液是碳酸钠;产生该现象的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑;该反应属于基本反应类型中的复分解反应,步骤①乙溶液中溶质一定有氯化钙.
(3)根据步骤③实验现象则上层溶液中一定含有的溶质是氯化钠(酸碱指示剂除外),可能含有的溶质是氯化钙为验证可能含有的溶质,应该补充的实验操作是取样,滴加碳酸钠溶液.
【定量分析】
(4)已知酚酞与硝酸银不反应,同学们利用反应废液缸中的上层清液来测定某硝酸银溶液中溶质的质量分数.取上层清液,滴加硝酸银溶液,产生沉淀的质量变化如图所示,该硝酸银溶液溶质的质量分数为10%.
12.下列洗涤方法中涉及到乳化作用的是( )
| A. | 用氢氧化钠溶液清洗盛装过植物油的瓶子 | |
| B. | 用酒精或汽油清洗掉衣服上的油污 | |
| C. | 用稀盐酸清洗盛装过石灰水的试剂瓶 | |
| D. | 加了餐具洗洁精的热水洗涤碗碟上的油污 |
9.“善待地球,保护环境,向污染宣战”是世界环境日的中国主题,为让成都天更蓝,地更绿,水更清,下列建议可行的是( )
| A. | 焚烧秸秆,增加肥力 | B. | 禁用农药,保护水资源 | ||
| C. | 回收塑料,再生减污 | D. | 深埋电池,消除污染 |
6.下列说法正确的是( )
| A. | 可燃冰能燃烧是因为其主要成分是甲烷 | |
| B. | 泡沫灭火器可用于扑灭电器引起的失火 | |
| C. | 雨水呈酸性的雨就是酸雨 | |
| D. | C02、CO、N02、S02都是有毒有害气体 |
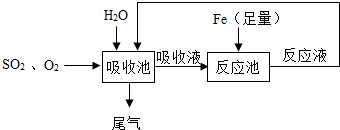 某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO2和O2混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环.
某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO2和O2混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环.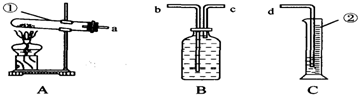
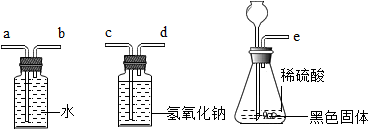 课外小科约老师继续探究铁粉和硫粉反应的实验:他们各自取一定量的铁粉和硫粉均匀混合后堆放在石棉网上,在其中插入烧红的玻璃棒,反应立即发生.拿掉玻璃棒后,反应继续剧烈进行,反应过程中有少量刺激性气味的气体X产生.反应结束后,都得到了黑色固体.老师得到的黑色固体不会被磁铁吸引,而小科的却会被磁铁吸引.
课外小科约老师继续探究铁粉和硫粉反应的实验:他们各自取一定量的铁粉和硫粉均匀混合后堆放在石棉网上,在其中插入烧红的玻璃棒,反应立即发生.拿掉玻璃棒后,反应继续剧烈进行,反应过程中有少量刺激性气味的气体X产生.反应结束后,都得到了黑色固体.老师得到的黑色固体不会被磁铁吸引,而小科的却会被磁铁吸引.