题目内容
6. 某校兴趣小组从废旧铝合金窗截下一块铝片,用托盘天平称其质量为27g,然后将它放入21.9%的稀盐酸中,产生氢气的质量与消耗盐酸的质量如图(假设该铝片中除表面含有氧化铝外,其他杂质不与酸反应且不含铝元素).请回答:
某校兴趣小组从废旧铝合金窗截下一块铝片,用托盘天平称其质量为27g,然后将它放入21.9%的稀盐酸中,产生氢气的质量与消耗盐酸的质量如图(假设该铝片中除表面含有氧化铝外,其他杂质不与酸反应且不含铝元素).请回答:(1)当稀盐酸的质量为250g时,产生的氢气的质量为1.2g.
(2)用化学方程式说明当稀盐酸的质量为50g时,为什么不产生氢气:
Al2O3+6HCl═2AlCl3+3H2O.
(3)计算该铝片中中铝元素的质量分数.(写出计算过程)
分析 (1)根据图象可知,放出氢气质量为1.2g;
(2)不产生氢气的原因是稀盐酸先和氧化铝反应;
(3)根据氢气的质量计算出单质铝的质量,根据氧化铝的质量计算出氧化铝中铝元素的质量,进而求质量分数.
解答 解:(1)图象为产生氢气质量随所加盐酸质量变化情况.根据图象可知,放出氢气质量为1.2g;故填:1.2;
(2)不产生氢气的原因是稀盐酸先和氧化铝反应,反应的化学方程式为:Al2O3+6HCl═2AlCl3+3H2O;故填:Al2O3+6HCl═2AlCl3+3H2O;
(3)解:设27g铝片中含铝的质量为x.
2Al+6HCl═2AlCl3+3H2↑
54 6
x 1.2g
$\frac{54}{6}$=$\frac{x}{1.2g}$
解得x=10.8g
设该铝片表面被氧化Al2O3的质量为y.
Al2O3+6HCl═2AlCl3+3H2O
102 6×36.5
y 50.0 g×21.9%
y=$\frac{50.0g×21.9%×102}{6×36.5}$=5.1 g
则氧化铝中铝元素的质量为$\frac{27×2}{102}$×5.1 g=2.7 g
被氧化的铝质量占未被氧化时铝片总质量的质量分数为$\frac{2.7g+10.8g}{27g}$×100%=50%
答:该铝片中中铝元素的质量分数为50%.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
16.下列化学反应中,既是置换反应又是还原反应的是( )
| A. | 煅烧石灰石 | B. | 氧化钙干燥剂吸潮 | ||
| C. | 用氢氧化钠溶液吸收二氧化碳 | D. | 木炭与氧化铜在高温下反应 |
17.下列变化中,氧元素以单质形式转变为化合物形式的是( )
| A. | 加热氯酸钾和二氧化锰的混合物制氧气 | |
| B. | 用高锰酸钾加热制取氧气 | |
| C. | 蜡烛在空气中燃烧生成二氧化碳和水 | |
| D. | 高温煅烧石灰石生成氧化钙和二氧化碳 |
14.下列民间制作属于化学变化的是( )
| A. | 阳朔画扇 | B. | 雁山竹编 | C. | 桂林辣椒酱 | D. | 瑶家小锅米酒 |
15.在厨房里里经常有下列变化发生,其中属于物理变化的是( )
| A. | 食物腐败 | B. | 开水沸腾 | C. | 液化气燃烧 | D. | 菜刀生锈 |
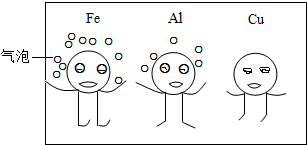 为验证Cu、Al、Fe三种金属的活动性顺序,有甲、乙、丙三位同学设计了如下方案:(溶液中Fe2+浅绿色、Cu2+蓝色、Al3+无色)
为验证Cu、Al、Fe三种金属的活动性顺序,有甲、乙、丙三位同学设计了如下方案:(溶液中Fe2+浅绿色、Cu2+蓝色、Al3+无色) 某长期暴露在空气中的氢氧化钠样品已部分变质,为了测定其纯度,现进行如下实验:取样品18g加入到足量水中充分搅拌至完全溶解,向所得溶液中逐滴滴加稀盐酸,产生气体的质量与所加稀盐酸质量的关系如图所示.分析题意并回答下列问题:
某长期暴露在空气中的氢氧化钠样品已部分变质,为了测定其纯度,现进行如下实验:取样品18g加入到足量水中充分搅拌至完全溶解,向所得溶液中逐滴滴加稀盐酸,产生气体的质量与所加稀盐酸质量的关系如图所示.分析题意并回答下列问题: