题目内容
6.某工厂与从含有CuSO4的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如图: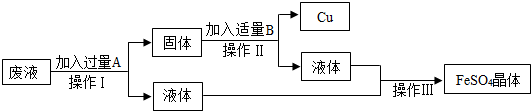
(1)操作Ⅰ的名称是过滤,需要用到的玻璃仪器除烧杯之外还有玻璃棒、漏斗操作Ⅲ蒸发.
(2)加入过量A物质的化学式是Fe
(3)加适量B物质的化学式是稀硫酸,加入适量B物质时反应的化学方程式是Fe+H2SO4=FeSO4+H2↑.
分析 根据在金属活动性顺序中,氢前的金属能与酸反应生成盐和氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,所以要回收铜得到硫酸亚铁,可以加入铁进行分析.
解答 解:(1)经过操作a能得到固体和液体,所以a操作为过滤,需要用到的玻璃仪器除烧杯之外还有玻璃棒、漏斗,从液体中得到晶体可以是蒸发操作;
(2)加入过量A物质的化学式是Fe;
(3)加适量B物质的化学式是稀硫酸,加入适量B物质时反应是铁和硫酸反应生成硫酸亚铁和氢气,化学方程式是:Fe+H2SO4=FeSO4+H2↑.
故答案为:(1)过滤,玻璃棒、漏斗,蒸发;
(2)Fe;
(3)稀硫酸,Fe+H2SO4=FeSO4+H2↑.
点评 本题考查了铜的回收,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
17.2014年6月5日是第43个“世界环境日”.下列做法不利于保护环境的是( )
| A. | 鼓励家庭生活垃圾分类收集 | |
| B. | 严禁焚烧秸秆,降低空气中PM2.5的浓度 | |
| C. | 发展低碳经济,减小火力发电站占总发电量的比例 | |
| D. | 用化工厂未达标排放的废水灌溉农田 |
14.在下列空格中写出有关的化学符号或表示的意义:
化学符号 | 2N | $\stackrel{+2}{Mg}$ | 3H2 | 2H2O |
表示意义 | 2个氮原子 | +2价的镁元素 | 3个氢分子 | 2个水分子 |
18.如图所示的实验操作不正确的是( )
| A. | 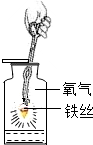 铁丝在氧气中的燃烧 | B. |  检验空气中氧气含量 | ||
| C. |  探究分子不断运动 | D. |  溶液滴定 |
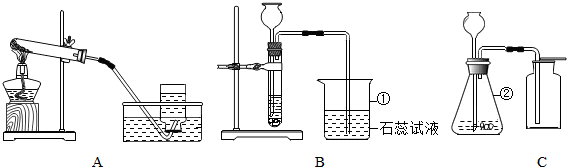
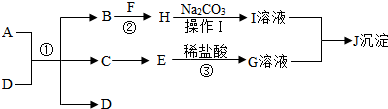 下列物质均为初中化学中常见的物质,其中A、B的组成元素相同,A、B、D、E、F为氧化物,H为改良酸性土壤常用的物质,如图是它们之间的转化关系,请回答:
下列物质均为初中化学中常见的物质,其中A、B的组成元素相同,A、B、D、E、F为氧化物,H为改良酸性土壤常用的物质,如图是它们之间的转化关系,请回答: