题目内容
11.化学源于生活,生活中蕴含许多化学知识.(1)硬水不宜洗涤衣物,家庭生活中可通过煮沸降低水的硬度.
(2)若水有臭味或色素可用活性炭除去.
(3)我们常用肥皂水区分硬水和软水.
(4)“节约用水,从我做起.”请你任举一例生活中节约用水的措施是淘米水浇花
(5)请写出一条防止太子河水体污染的措施工业废水经过处理净化达标后再排放.
分析 (1)根据生活中降低水的硬度的方法分析;
(2)根据活性炭具有吸附性,能吸附异味和色素进行分析;
(3)根据硬水软水的检测方法分析;
(4)根据节约用水的方法分析;
(5)根据常见的防止水污染的措施分析回答.
解答 解:(1)硬水不宜洗涤衣物,家庭生活中可通过煮沸降低水的硬度.
(2)若水有臭味或色素可用活性炭除去.
(3)可用肥皂水鉴别硬水和软水,其中产生泡沫较多的是软水,泡沫较少的是硬水;
(4)生活中节约用水的措施很多,例如:淘米水浇花;洗菜的水用来冲厕所;使用节水龙头等.
(5)防止河水污染的有效措施有:工业废水经过处理净化达标后再排放,农业上合理使用化肥和农药等.
故答案是:(1)煮沸;(2)活性炭;(3)肥皂水;(4)淘米水浇花;(5)工业废水经过处理净化达标后再排放.
点评 本题难度不大,物质的性质决定物质的用途,掌握常见化学物质的性质和用途是正确解答此类题的关键.解答本题要充分理解各种净化水的方法以及水的污染和防止污染的措施的知识,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案
相关题目
16.从事中药和中西药结合研究的屠呦呦,创造性地研制出抗疟新药--青蒿素(化学式:C15H22O5),获2015年诺贝尔生理学或医学奖,成为第一个获得诺贝尔自然学奖的中国人.下列关于青蒿素的说法中正确的是( )
| A. | 青蒿素相对分子质量为282g | |
| B. | 青蒿素由15个碳原子、22个氢原子和5个氧原子构成 | |
| C. | 碳、氢、氧三种元素的质量比为90:11:40 | |
| D. | 青蒿素中氢元素的质量分数最大 |
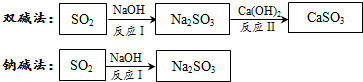
3.工业烟气通常含二氧化硫,在排放前需经脱硫处理.如图是两种常用脱硫工艺中含硫物质的转化路径(部分产物已略).
(1)下列环境问题与SO2有关的是A(填字母序号).
A.酸雨 B.温室效应 C.臭氧空洞
(2)双碱法中的“双碱”指的是Ca(OH)2和NaOH(填化学式).
(3)写出反应Ⅰ的化学方程式:SO2+2NaOH=Na2SO3+H2O.
(4)反应Ⅱ所属的基本反应类型是复分解反应.
(5)已知部分原料的价格如下表所示.
两种工艺中,处理相同量的SO2,双碱法所需的原料成本更低,原因是通过反应II实现了NaOH的循环利用,减少了NaOH的用量,所以成本降低(物质组成和变化分析).

(1)下列环境问题与SO2有关的是A(填字母序号).
A.酸雨 B.温室效应 C.臭氧空洞
(2)双碱法中的“双碱”指的是Ca(OH)2和NaOH(填化学式).
(3)写出反应Ⅰ的化学方程式:SO2+2NaOH=Na2SO3+H2O.
(4)反应Ⅱ所属的基本反应类型是复分解反应.
(5)已知部分原料的价格如下表所示.
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.90 |
20.从化学的视角认识下列食物中富含蛋白质的是( )
| A. |  米饭 | B. |  西红柿 | C. |  牛肉 | D. |  花生油 |
1.化学调研小组的同学用氢氧化钠和稀盐酸探究中和反应,请你参与以下探究:

(1)甲组同学取少量的氢氧化钠溶液于烧杯中,用酸度计测得该溶液的pH同时插入一支温度计,测量溶液的温度(如图1示).用胶头滴管吸取稀盐酸,逐滴加入盛有氢氧化钠溶液的烧杯中,边滴加边搅拌.此时可观察到的现象是:酸度计上显示的数据逐渐减少(选填“增大”、“减少”或“不变”),温度计上显示的数据逐渐升高,由此可知,酸和碱的中和反应属于放热(选填“吸热”或“放热”)反应.
(2)乙组的同学改用固体氢氧化钠与稀盐酸反应来探究中和反应中能量的变化情况,你认为该方案不合理(选填“合理”或“不合理”),原因固体氢氧化钠溶于水会放出热量.
(3)丙组同学用另外一瓶氢氧化钠溶液进行实验时,当往烧杯中滴加稀盐酸时,发现有少量的气泡冒出,小组同学根据这一现象进行讨论,一致认为其原因可能是氢氧化钠溶液已经变质,原因是CO2+2NaOH═Na2CO3+H2O(写化学方程式)
(4)丁组同学借助酚酞试液来判断氢氧化钠溶液与稀盐酸发生中和反应时,在烧杯中加入氢氧化钠溶液后,滴几滴酚酞溶液,然后加入一定量稀盐酸,最后溶液为无色.小金认为溶液显中性.小东认为不一定.小东同学设计以下实验进行了验证,结果否定小金的结论:
(5)戊组同学对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为20%的氢氧化钠溶液进行中和,如图2示.请你计算废水中盐酸的溶质质量分数.(写出具体的计算过程 )

(1)甲组同学取少量的氢氧化钠溶液于烧杯中,用酸度计测得该溶液的pH同时插入一支温度计,测量溶液的温度(如图1示).用胶头滴管吸取稀盐酸,逐滴加入盛有氢氧化钠溶液的烧杯中,边滴加边搅拌.此时可观察到的现象是:酸度计上显示的数据逐渐减少(选填“增大”、“减少”或“不变”),温度计上显示的数据逐渐升高,由此可知,酸和碱的中和反应属于放热(选填“吸热”或“放热”)反应.
(2)乙组的同学改用固体氢氧化钠与稀盐酸反应来探究中和反应中能量的变化情况,你认为该方案不合理(选填“合理”或“不合理”),原因固体氢氧化钠溶于水会放出热量.
(3)丙组同学用另外一瓶氢氧化钠溶液进行实验时,当往烧杯中滴加稀盐酸时,发现有少量的气泡冒出,小组同学根据这一现象进行讨论,一致认为其原因可能是氢氧化钠溶液已经变质,原因是CO2+2NaOH═Na2CO3+H2O(写化学方程式)
(4)丁组同学借助酚酞试液来判断氢氧化钠溶液与稀盐酸发生中和反应时,在烧杯中加入氢氧化钠溶液后,滴几滴酚酞溶液,然后加入一定量稀盐酸,最后溶液为无色.小金认为溶液显中性.小东认为不一定.小东同学设计以下实验进行了验证,结果否定小金的结论:
| 实验步骤 | 实验现象 | 结论 |
| 取少量反应后的溶液于试管中,滴加几滴紫色的石蕊试液 | 石蕊试液变红色 | 没有完全中和 |