题目内容
15.某兴趣小组利用如图所示装置进行有关性质的研究.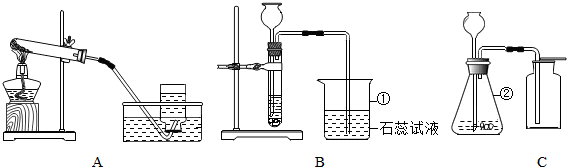
(1)写出下列编号仪器的名称:①烧杯,②锥形瓶.
(2)甲同学要用高锰酸钾来制取O2,应选用图中的A装置(填编号),该反应的化学方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)查阅资料知:浓盐酸具有挥发性,能挥发出氯化氢.
①乙同学用浓盐酸和大理石在B装置中反应,制取CO2并检验其有关性质时观察到烧杯中紫色石蕊试液变红.对这一变化的合理解释有BC(填序号).
A.产生的CO2直接使石蕊试液变红
B.产生的CO2与水反应生成H2CO3使石蕊试液变红
C.挥发出的氯化氢溶于水使石蕊试液变红
②乙同学将制得的气体通入澄清的石灰水中,石灰水没有变浑浊,其原因是CO2中混有HCl气体.
(4)丙同学用C装置制取了一瓶无色、无味的气体(纯净物),你推测该气体可能是O2(合理均可),试用最简便的方法证实你的推测将带火星的木条放在集气瓶内,若木条复燃,说明是氧气.
分析 (1)据常用化学仪器及名称解答;
(2)根据用高锰酸钾制取氧气是固体的加热反应,选择发生装置,并据反应原理书写方程式;
(3)①根据浓盐酸易挥发和二氧化碳的性质及酸性溶液可使石蕊变红进行解答;
②石灰水没有变浑浊,说明通入的气体不是纯净的二氧化碳;制取二氧化碳时使用具有较强挥发性的浓盐酸,因此所产生的二氧化碳中混有氯化氢气体;
(4)根据发生装置和收集装置的特点选择制取的气体及检验的方法解答.
解答 解:(1)图中①是烧杯,②是锥形瓶;
(2)用高锰酸钾制取氧气是固体的加热反应,可以用装置A作为发生装置,反应的方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)①酸可以使石蕊试液变红,乙同学用浓盐酸和大理石在B装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红.可能的原因有:产生的CO2与水反应生成H2CO3使石蕊试液变红;挥发出的氯化氢溶于水使石蕊试液变红;
②制得的气体通入澄清的石灰水中,石灰水没有变浑浊,因为挥发出的HCl气体与石灰水反应;
(4)C装置适用于固体和液体的不加热反应,可以用大理石和稀盐酸反应制取二氧化碳,也可以用双氧水和二氧化锰反应制取氧气,检验的方法是:将带火星的木条放在集气瓶内,若木条复燃,说明是氧气(或向集气瓶内倒入适量的石灰水,若石灰水变浑浊,说明是二氧化碳);
故答案为:(1)烧杯; 锥形瓶;
(2)A; 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)BC; CO2中混有HCl气体;
(4)O2(合理均可);将带火星的木条放在集气瓶内,若木条复燃,说明是氧气.
点评 本题考查气体的制取综合性较强,实验仪器的选择、装置的选择、化学方程式的书写、气体的检验等内容,是中考中经常考查的内容,同学们一定要掌握好.

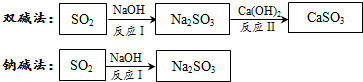
(1)下列环境问题与SO2有关的是A(填字母序号).
A.酸雨 B.温室效应 C.臭氧空洞
(2)双碱法中的“双碱”指的是Ca(OH)2和NaOH(填化学式).
(3)写出反应Ⅰ的化学方程式:SO2+2NaOH=Na2SO3+H2O.
(4)反应Ⅱ所属的基本反应类型是复分解反应.
(5)已知部分原料的价格如下表所示.
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.90 |
| A. | pH<5.6的雨水称为酸雨 | |
| B. | 葡萄糖是一种有机物,是人体内重要的提供能量的物质 | |
| C. | 在葡萄糖中加硫酸铜溶液,加热到沸腾,出现红色沉淀 | |
| D. | 食用甲醛浸泡的食物对人体有害 |
| A. |  米饭 | B. |  西红柿 | C. |  牛肉 | D. |  花生油 |
| A. | 自来水通过蒸馏变成可饮用的瓶装蒸馏水 | |
| B. | 夜幕降临,霓虹灯通电后发出美丽的亮光 | |
| C. | 青铜受热融化后浇铸成各种形状的工艺品 | |
| D. | 用乙醇汽油做燃料驱动汽车 |
| A. | 不同元素的根本区别在于其相对原子质量不同 | |
| B. | 分子是化学变化中的最小粒子 | |
| C. | 氧化物一定含有氧元素 | |
| D. | 带电的粒子一定是离子 |
(1)管道煤气的主要成分是CO和少量碳氢化合物,天然气的主要成分是CH4,它们的燃烧反应如下:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
已知在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子,试根据以上方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是天然气,因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进的方法是增大进气口(填“增大”或“减小”),如不加改进可能产生的不良后果是有毒的CO生成,甚至有固体残留物堵塞燃气管道.
(2)液化石油气的主要成分是丙烷(C3H8)、丁烷(C4H10)等,它们的某些性质见下表:
| 乙烷(C2H6) | 丙烷(C3H8) | 丁烷(C4H10) | |
| 熔点(℃) | -183.3 | -189.7 | -138.4 |
| 沸点(℃) | -88.6 | -42.1 | -0.5 |
有趣的是,使用液化石油气的居民在改用天然气时,也将涉及灶具的调整,已知碳氢化合物充分燃烧的产物跟甲烷相同,请根据液化石油气的燃烧方程式,说明灶具改进的方法:将进气口增大.