题目内容
1.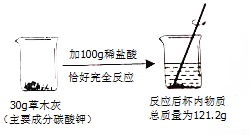 草木灰是农家肥料,其主要成分是碳酸钾,某化学兴趣小组进行如图实验,以下是他们的实验过程及数据(假设杂质不与稀盐酸反应,生成的气体全部逸出).请你回答下列问题:
草木灰是农家肥料,其主要成分是碳酸钾,某化学兴趣小组进行如图实验,以下是他们的实验过程及数据(假设杂质不与稀盐酸反应,生成的气体全部逸出).请你回答下列问题:(1)碳酸钾中钾元素、碳元素、氧元素的质量比为39:6:24;
(2)反应后生成的气体质量为8.8g;
(3)稀盐酸中溶质质量分数是多少?
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;
(2)根据图中的数据,进行分析;
(3)根据二氧化碳的质量可以计算反应生成氯化氢的质量,进一步可以计算稀盐酸中溶质质量分数.
解答 解:
(1)碳酸钾中钾元素、碳元素、氧元素的质量比为(39×2):12:(16×3)=39:6:24;
(2)反应后生成的气体质量为30g+100g-121.2g=8.8g;
(3)设稀盐酸中溶质氯化氢的质量为x.
K2CO3+2HCl=2KCl+CO2↑+H2O.
73 44
x 8.8g
则$\frac{73}{44}=\frac{x}{8.8g}$,解得x=14.6g.
故稀盐酸中溶质的质量分数为$\frac{14.6g}{100g}×100%$=14.6%.
故答案为:
(1)39:6:24;(2)8.8g;(3)14.6%.
点评 本题难度不大,掌握化合物中元素质量比的计算方法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
12.下列用于改正错别字的方法中,与另外三种有本质区别的方法是( )
| A. |  用橡皮擦去 | B. |  用透明胶带粘除 | C. |  用修正纸覆盖 | D. |  用退字灵改写 |
6.学习化学的一个重要途径是科学探究,实验是科学探究的重要手段,下列化学实验操作正确的是( )
| A. | 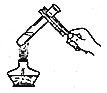 加热液体 | B. | 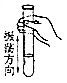 振荡试管 | C. | 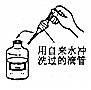 放回滴瓶 | D. |  检查气密性 |
10.下列各组物质,能在水中形成无色透明溶液的一组是( )
| A. | NaOH、FeCl3、MgSO4、NaCl | B. | KCl、HCl、CuSO4、KNO3 | ||
| C. | Na2SO4、NaOH、HCl、KCl | D. | Na2CO3、KNO3、NaCl、CaCl2 |
10.下列关于原子核的说法正确的是( )
| A. | 原子核由质子和电子构成 | B. | 原子核由质子和中子构成 | ||
| C. | 原子核由质子、电子和中子构成 | D. | 原子核带负电 |
 某粒子R的结构示意图为:
某粒子R的结构示意图为: 泉水是“泉城”济南的文化之魂.首届济南泉水节拟于2013年8月28日开幕.节水环保、杜绝水污染、建设美丽地球是我们的职责
泉水是“泉城”济南的文化之魂.首届济南泉水节拟于2013年8月28日开幕.节水环保、杜绝水污染、建设美丽地球是我们的职责