题目内容
3.我们熟知氢氧化钠是一种重要的碱.它可以和许多物质发生化学反应,常用于造纸、炼油、纺织、印染与橡胶等.小春同学用如图总结了氢氧化钠的四条化学性质.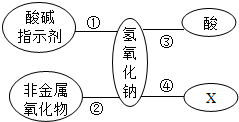
回答下列问题:
(1)X为盐.
(2)完成如图中标号所对应的化学反应方程式:
②2NaOH+CO2=Na2CO3+H2O.
③HCl+NaOH=NaCl+H2O,基本类型复分解反应.
④FeCl3+3NaOH═Fe(OH)3↓+3NaCl.
分析 (1)根据氢氧化钠的性质分析X;
(2)根据氢氧化的性质写出反应的化学方程式,根据反应的特点分析反应的类型.
解答 解:(1)氢氧化钠是一种碱,能与酸碱指示剂、某些非金属氧化物和某些盐反应,所以X应是盐;
(2)②氢氧化钠能与某些非金属氧化物反应,所以②可以为:2NaOH+CO2=Na2CO3+H2O;
③氢氧化钠能与酸发生中和反应,所以③可以为:HCl+NaOH=NaCl+H2O,该反应由两种化合物相互交换成分生成了两种新的化合物,属于复分解反应;
④氢氧化钠能与某些盐发生反应,所以④可以为:FeCl3+3NaOH═Fe(OH)3↓+3NaCl.
故答为:(1)盐;(2)②2NaOH+CO2=Na2CO3+H2O;
③HCl+NaOH=NaCl+H2O,复分解反应;
④FeCl3+3NaOH═Fe(OH)3↓+3NaCl.
点评 本题难度不大,考查氢氧化钠的性质、根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.下列实验操作中,正确的是( )
| A. | 用滴管滴加液体时,滴管下端要紧贴试管内壁 | |
| B. | 加热试管中的液体应直接加热,不必进行预热 | |
| C. | 用100mL的量筒量取10mL液体 | |
| D. | 向试管里倾倒液体时,试剂瓶紧挨试管口 |
14. 某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.
某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.
探究1:研究常见的物质--氢氧化钠和盐酸的反应程度.
探究2:研究酸的性质--硫酸、盐酸和锌反应通过探究实验,同学们发现硫酸和盐酸溶液都可以和锌反应产生氢气.产生这种共同现象的原因为硫酸和盐酸溶液中都含有氢离子.
探究3:探索未知--浓硝酸和铜制取气体.
已知Cu+4HNO3(浓)═Cu(NO3)2+2H2O+2NO2↑.NO2能和水反应生成硝酸和NO.NO和NO2都是空气的污染物.
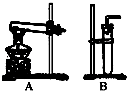
(1)利用该反应制取二氧化氮,其发生装置应选用右图所示装置中的.收集NO2的方法为向上排空气法.
(2)NO为无色气体,其和空气接触会变为红棕色,这是因为NO和空气中的氧气发生化合反应生成了NO2,其反应的化学方程式为:2NO+O2═2N02
探究4:兴趣小组同学向盛有澄清石灰水1000g的大烧杯中加入10g碳酸钠溶液,恰好完全反应后过滤去沉淀,剩余液体总质量为1009.8g,请你计算所加碳酸钠溶液的溶质质量分数?
 某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.
某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.探究1:研究常见的物质--氢氧化钠和盐酸的反应程度.
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入固体化合物. | (加CaCO3),有气泡产生. | 盐酸过量 |
探究3:探索未知--浓硝酸和铜制取气体.
已知Cu+4HNO3(浓)═Cu(NO3)2+2H2O+2NO2↑.NO2能和水反应生成硝酸和NO.NO和NO2都是空气的污染物.
(1)利用该反应制取二氧化氮,其发生装置应选用右图所示装置中的.收集NO2的方法为向上排空气法.
(2)NO为无色气体,其和空气接触会变为红棕色,这是因为NO和空气中的氧气发生化合反应生成了NO2,其反应的化学方程式为:2NO+O2═2N02
探究4:兴趣小组同学向盛有澄清石灰水1000g的大烧杯中加入10g碳酸钠溶液,恰好完全反应后过滤去沉淀,剩余液体总质量为1009.8g,请你计算所加碳酸钠溶液的溶质质量分数?
11.下列属于人体中微量元素的是( )
| A. | 钙 | B. | 氧 | C. | 氮 | D. | 硒 |
18.若按照如图所示实验方案分离氯化钡和氯化钠的固体混合物,则X溶液中的溶质是( )
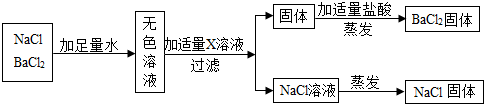

| A. | 碳酸钾 | B. | 碳酸钠 | C. | 硫酸钠 | D. | 氢氧化钠 |
8.下列做法或认识是正确的是( )
| A. | 垃圾经分类回收处理可转化为资源 | |
| B. | 煤气中毒应大量喝牛奶 | |
| C. | 用硬水洗衣服比用软水洗效果好 | |
| D. | 厨房煤气泄漏,立即打开排气扇电源 |
13.下列应用中,主要使用复合材料的是( )
| A. | 使用碳纤维制作的赛艇 | B. | 使用棉质的T恤 | ||
| C. | 使用铁合金制作的标枪 | D. | 使用合成纤维制作的泳衣 |
 如图所示,A~H是初中化学常见的物质,A和B可发生中和发应,X常用作食品干燥剂,Y为单质.根据图示回答下列问题:
如图所示,A~H是初中化学常见的物质,A和B可发生中和发应,X常用作食品干燥剂,Y为单质.根据图示回答下列问题: