题目内容
16. 如表提供了A、B两种物质的溶解度数据,读取信息后回答:
如表提供了A、B两种物质的溶解度数据,读取信息后回答:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 物质A | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 |
| 物质B | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(2)A、B两物质溶解度随温度变化趋势的不同是:A的溶解度变化小,B的溶解度变化大;
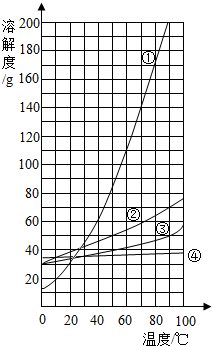
(3)如图给出的曲线中,③与A物质溶解度的变化趋势相符(填曲线编号);
(4)从A、B两物质的混合物中分离出B物质,一般采用降温结晶的方法.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)在20℃时,A物质的溶解度是34g,B物质的溶解度是31.6g,所以A、B物质都属于易溶物质;
(2)通过分析溶解度表中的数据可知,A、B两物质溶解度随温度变化趋势的不同是:A的溶解度变化小,B的溶解度变化大;
(3)物质A的溶解度受温度影响较小,在80℃时的溶解度是51.1g,所以③与A物质溶解度的变化趋势相符;
(4)B物质的溶解度受温度影响较大,所以从A、B两物质的混合物中分离出B物质,一般采用降温结晶的方法.
故答案为:(1)易溶;
(2)A的溶解度变化小,B的溶解度变化大;
(3)③;
(4)降温结晶.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
4.现有一块合金质量为35克,使它与足量稀硫酸完全反应后,生成2克氢气,则此合金的组成元素不可能为( )
| A. | Zn和Al | B. | Al和Mg | C. | Mg和Fe | D. | Mg和Cu |
11.小红对爸爸给患病的奶奶购买的“便携式制氧器”产生了兴趣,她阅读说明书,了解了它的工作原理(如图1)和所用药品.药品中甲剂是一种白色颗粒状固体,作制氧剂;乙剂是黑色固体,作催化剂.甲剂、乙剂和水盛放在图1的反应仓中.

【提出问题】甲剂的化学成分是什么?
【查阅资料】过碳酸钠是一种白色颗粒状固体,溶于水时,生成碳酸钠和过氧化氢. 可用于制取氧气.
【设计与实验】小红把甲剂和乙剂带到实验室与姜老师共同探究.在老师的指导下,验证出甲剂是一种钠盐后,小红接着进行如下实验:
【实验一】用甲剂、乙剂和水制取并验证氧气.
(1)根据图1和图2回答问题:
①写出图2中标有a、b的仪器名称:a酒精灯;b试管.
②请指出小红在实验中制取氧气时,应选用的发生装置为B(填字母).
③收集氧气时,由于它具有密度大于空气的性质,则可选用的气体收集装置是C(填字母).
(2)将带火星的木条伸入到集气瓶内,若带火星的木条复燃,则说明收集到的气体是氧气.
(3)小红认为氧气是由过氧化氢,在乙剂催化作用下产生的,其化学方程式为:2H2O2$\stackrel{乙剂}{=}$2H2O+O2↑.
【实验二】检验[实验一]反应后的溶液中是否含有某种离子.
【实验结论】
(1)【实验一】反应后的溶液中一定含有较多钠离子和氯 离子.
(2)甲剂可能是过碳酸钠.

【提出问题】甲剂的化学成分是什么?
【查阅资料】过碳酸钠是一种白色颗粒状固体,溶于水时,生成碳酸钠和过氧化氢. 可用于制取氧气.
【设计与实验】小红把甲剂和乙剂带到实验室与姜老师共同探究.在老师的指导下,验证出甲剂是一种钠盐后,小红接着进行如下实验:
【实验一】用甲剂、乙剂和水制取并验证氧气.
(1)根据图1和图2回答问题:
①写出图2中标有a、b的仪器名称:a酒精灯;b试管.
②请指出小红在实验中制取氧气时,应选用的发生装置为B(填字母).
③收集氧气时,由于它具有密度大于空气的性质,则可选用的气体收集装置是C(填字母).
(2)将带火星的木条伸入到集气瓶内,若带火星的木条复燃,则说明收集到的气体是氧气.
(3)小红认为氧气是由过氧化氢,在乙剂催化作用下产生的,其化学方程式为:2H2O2$\stackrel{乙剂}{=}$2H2O+O2↑.
【实验二】检验[实验一]反应后的溶液中是否含有某种离子.
| 实验步骤 | 实验操作 | 实验现象 | 化学反应方程式 |
| 步骤一 | 取少量反应后的溶液,加入稀盐酸 | 有气泡产生 | |
| 步骤二 | 将步骤一产生的气体通入澄清的石灰水中 | 澄清石灰水变浑浊 | CO2+Ca(OH)2═CaCO3↓+H2O |
(1)【实验一】反应后的溶液中一定含有较多钠离子和氯 离子.
(2)甲剂可能是过碳酸钠.
1.馒头遇到固态碘、碘溶液和碘蒸气都能变蓝色,这一实验现象说明( )
| A. | 分子是保持物质化学性质的最小粒子 | |
| B. | 原子是化学变化中的最小粒子 | |
| C. | 分子是构成物质的一种粒子 | |
| D. | 化学变化中分子可分成原子 |
8. 如图表示某反应前后反应物与生成物分子及其数目变化,其中“
如图表示某反应前后反应物与生成物分子及其数目变化,其中“ ”“
”“ ”“
”“ ”分别表示A、B、C三种不同的分子.则该反应的化学方程式中A、B、C前的化学计量数之比为( )
”分别表示A、B、C三种不同的分子.则该反应的化学方程式中A、B、C前的化学计量数之比为( )
 如图表示某反应前后反应物与生成物分子及其数目变化,其中“
如图表示某反应前后反应物与生成物分子及其数目变化,其中“ ”“
”“ ”“
”“ ”分别表示A、B、C三种不同的分子.则该反应的化学方程式中A、B、C前的化学计量数之比为( )
”分别表示A、B、C三种不同的分子.则该反应的化学方程式中A、B、C前的化学计量数之比为( )| A. | 4:1:4 | B. | 4:1:2 | C. | 2:1:2 | D. | 1:2:2 |
5.回答下列问题:
(1)碳酸钠是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料,它属于盐(填“酸”、“碱”或“盐”),它的俗名叫纯碱的原因是碳酸钠的水溶液显碱性.
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为Ca(OH)2+2NH4Cl=CaCl2+2NH3↑+2H2O,制取和收集氨气可用下图中的A和D装置.

(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
请你据此分析计算:
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是1.8g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(1)碳酸钠是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料,它属于盐(填“酸”、“碱”或“盐”),它的俗名叫纯碱的原因是碳酸钠的水溶液显碱性.
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为Ca(OH)2+2NH4Cl=CaCl2+2NH3↑+2H2O,制取和收集氨气可用下图中的A和D装置.

(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质的总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是1.8g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)

 表示氯原子,
表示氯原子, 表示氧原子,
表示氧原子, 表示氢原子)
表示氢原子)