题目内容
8.某中学化学实验室有如图所示的实验装置,用于制取氧气、二氧化碳等多种气体.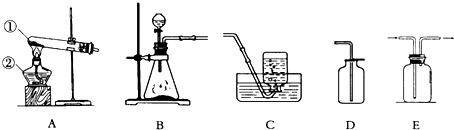
(1)请写出有标号仪器的名称:①试管;②酒精灯
(2)用A装置制取氧气,发生反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,若要收集较纯净的氧气,应选用的收集装置是C(填代号,下同),将药品加入装置A中的试管前,应进行的操作是检查装置的气密性;
(3)实验室制CO2的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑,应选择的发生装置是(填代号)B,若选用E装置,采用排空气法收集CO2时,气体应从(填“左端”或“右端”)左端口进入,原因是二氧化碳的密度比空气大
(4)在常温下,用硫化亚铁固体和稀硫酸制取硫化氢气体,应选用的发生装置是:B;由于硫化氢是密度比空气大,有毒且能溶于水的酸性气体,所以应用E装置进行收集,以便将尾气吸收处理,避免造成大气污染.实验室可用氢氧化钠溶液来吸收硫化氢气体.
分析 (1)据常用仪器回答;
(2)A装置是加热固体制取氧气,且试管口有棉花,是用加热高锰酸钾制取氧气,据反应原理书写方程式,收集纯净的氧气用排水发生法,药品加入前要检查装置的气密性,防止装置漏气;
(3)实验室制取二氧化碳用大理石和稀盐酸反应,据反应原理书写方程式,该反应属于固液常温型,故选发生装置B,二氧化碳密度比空气大,故要从长管进气;
(4)根据实验室制取硫化氢气体的反应原理,由原理反应所需要的条件,选择发生装置,利用硫化氢气体的性质,判断收集该气体的装置.
解答 解:(1)标号仪器分别是试管和酒精灯;
(2)A装置是加热固体制取氧气,且试管口有棉花,是用加热高锰酸钾制取氧气,反应的化学方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;收集纯净的氧气用排水发生法,药品加入前要检查装置的气密性,防止装置漏气;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳密度比空气大,故要从长管进气,将空气挤压到集气瓶上部排出;
(4)硫化亚铁固体和稀硫酸在常温下反应可制取硫化氢气体,因此发生装置应选B,由于硫化氢是密度比空气大,有毒且能溶于水的酸性气体,因此为防止有毒的硫化氢气体逸出造成空气污染,可使用装置E进行收集,以便于处理尾气;
故答案为:(1)试管;酒精灯;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;C;检查装置的气密性;
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;B;左端;二氧化碳的密度比空气大;
(4)B; E; 空气污染.
点评 本题主要考查了实验室制取氧气、二氧化碳的反应原理、装置选取、及常用仪器等知识,掌握相关知识才能正确解答,能较好考查学生分析、解决问题的能力.

 智能训练练测考系列答案
智能训练练测考系列答案| 实验步骤 | 实验现象 | 结论 | |
| 物理方法 | 将混合物放入盛有水的烧杯中 | 部分黑色粉末浮在水面上,部分沉在底部 | 将浮在水面上的黑色粉末慢慢倒出,然后将氧化铜过滤出来,干燥即可 |
| 化学方法 | 在空气中充分加热固体混合物 | 黑色固体减少 | 余下的黑色固体即为氧化铜 |
| A. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | B. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2 | ||
| C. | HgO$\frac{\underline{\;\;△\;\;}}{\;}$Hg+O2↑ | D. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO |
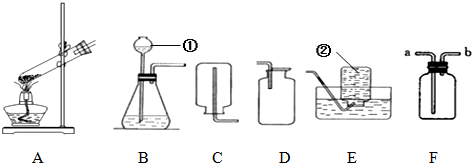
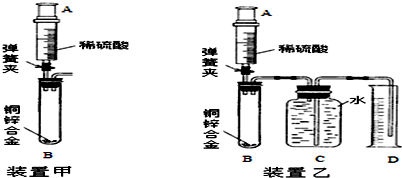
 水是一种重要的物质,在实验室和日常生活中有着十分重要的作用,但有时也会干扰我们的生活.请根据下列提示回答问题:
水是一种重要的物质,在实验室和日常生活中有着十分重要的作用,但有时也会干扰我们的生活.请根据下列提示回答问题: